Lees meer in de onderliggende hoofdstukken.
3 Preventie, Signaleren en verwijzen.
JGZ-richtlijn Voedselovergevoeligheid
JGZ-richtlijn Voedselovergevoeligheid
Let op: deze richtlijn is momenteel in herziening.
Dit betekent niet dat de inhoud van deze richtlijn incorrect is. Tot de herziening blijft de richtlijn leidend voor de praktijk. Wel bestaat er een kans dat een deel van de informatie verouderd is.
Heb je feedback over deze JGZ-richtlijn? Stuur jouw feedback naar onze servicedesk. Zoek het tekstgedeelte waarbij je suggesties voor verbetering hebt. Via de knop ‘Geef jouw feedback’ kun je voor deze JGZ-richtlijn en het specifieke hoofdstuk jouw suggesties doorgeven.
Richtlijn inhoudsopgave
1 Inleiding Ga naar pagina over 1 Inleiding
2 Definitie en achtergrondinformatie Ga naar pagina over 2 Definitie en achtergrondinformatie
3 Preventie, Signaleren en verwijzen. Ga naar pagina over 3 Preventie, Signaleren en verwijzen.
4 Begeleiden en behandelen Ga naar pagina over 4 Begeleiden en behandelen
5 Totstandkoming Ga naar pagina over 5 Totstandkoming
6 Verantwoording Ga naar pagina over 6 Verantwoording
1 Inleiding Ga naar pagina over 1 Inleiding
2 Definitie en achtergrondinformatie Ga naar pagina over 2 Definitie en achtergrondinformatie
3 Preventie, Signaleren en verwijzen. Ga naar pagina over 3 Preventie, Signaleren en verwijzen.
4 Begeleiden en behandelen Ga naar pagina over 4 Begeleiden en behandelen
5 Totstandkoming Ga naar pagina over 5 Totstandkoming
6 Verantwoording Ga naar pagina over 6 Verantwoording
Heb je suggesties voor verbetering van deze JGZ-richtlijn?
Geef jouw feedbackRichtlijn Voedselovergevoeligheid Samenvatting
Overzichtskaart richtlijn Voedselovergevoeligheid
PP-presentatie voor de scholing Voedselovergevoeligheid
Factsheet richtlijn Voedselovergevoeligheid
Randvoorwaardelijke implicaties richtlijn Voedselovergevoeligheid
Rapportage praktijktest richtlijn Voedselovergevoeligheid
BDS-registratie-protocol richtlijn Voedselovergevoeligheid
Bijlage 2b Beoordelingsformulier DBPGVP
Bijlage 2c Beoordelingsformulier Open koemelkprovocatie
Bijlage 2d Aanvraagformulier dieetpreparaat ziektekostenverzekeraar
Bijlage 2e Stroomschema diagnostiek koemelkallergie bij kinderen
Formulier voor allergische reacties na provocatietest
[1] American Academy of Pediatrics. Committee on Nutrition. Hypoallergenic infant formulas. Pediatrics 2000;106(2 Pt 1):346-9
https://pubmed.ncbi.nlm.nih.gov/10920165[2] . AGA Institute Medical Position Statement on the Diagnosis and Management of Celiac Disease. Gastroenterology 2006;131(6):1977-80
https://pubmed.ncbi.nlm.nih.gov/17087935[3] Aardoom HA, Hirasing RA, Rona RJ, Sanavro FL, van den Heuvel EW, Leeuwenburg J. Food intolerance (food hypersensitivity) and chronic complaints in children: the parents' perception. European journal of pediatrics 1997;156(2):110-2
https://pubmed.ncbi.nlm.nih.gov/9039513[4] Abrahamsson TR, Jakobsson T, Böttcher MF, Fredrikson M, Jenmalm MC, Björkstén B, Oldaeus G. Probiotics in prevention of IgE-associated eczema: a double-blind, randomized, placebo-controlled trial. The Journal of allergy and clinical immunology 2007;119(5):1174-80
https://pubmed.ncbi.nlm.nih.gov/17349686[5] Agostoni C, Fiocchi A, Riva E, Terracciano L, Sarratud T, Martelli A, Lodi F, D'Auria E, Zuccotti G, Giovannini M. Growth of infants with IgE-mediated cow's milk allergy fed different formulas in the complementary feeding period. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2007;18(7):599-606
https://pubmed.ncbi.nlm.nih.gov/17561927[6] Akobeng AK, Ramanan AV, Buchan I, Heller RF. Effect of breast feeding on risk of coeliac disease: a systematic review and meta-analysis of observational studies. Archives of disease in childhood 2006;91(1):39-43
https://pubmed.ncbi.nlm.nih.gov/16287899[7] Arslanoglu S, Moro GE, Schmitt J, Tandoi L, Rizzardi S, Boehm G. Early dietary intervention with a mixture of prebiotic oligosaccharides reduces the incidence of allergic manifestations and infections during the first two years of life. The Journal of nutrition 2008;138(6):1091-5
https://pubmed.ncbi.nlm.nih.gov/18492839[8] Ascher H, Krantz I, Rydberg L, Nordin P, Kristiansson B. Influence of infant feeding and gluten intake on coeliac disease. Archives of disease in childhood 1997;76(2):113-7
https://pubmed.ncbi.nlm.nih.gov/9068298[9] Auricchio S, Follo D, de Ritis G, Giunta A, Marzorati D, Prampolini L, Ansaldi N, Levi P, Dall'Olio D, Bossi A. Does breast feeding protect against the development of clinical symptoms of celiac disease in children? Journal of pediatric gastroenterology and nutrition 1983;2(3):428-33
https://pubmed.ncbi.nlm.nih.gov/6620050[10] Bardare M, Vaccari A, Allievi E, Brunelli L, Coco F, de Gaspari GC, Flauto U. Influence of dietary manipulation on incidence of atopic disease in infants at risk. Annals of allergy 1993;71(4):366-71
https://pubmed.ncbi.nlm.nih.gov/8214801[11] Barker JM. Clinical review: Type 1 diabetes-associated autoimmunity: natural history, genetic associations, and screening. The Journal of clinical endocrinology and metabolism 2006;91(4):1210-7
https://pubmed.ncbi.nlm.nih.gov/16403820[12] Bateman B, Warner JO, Hutchinson E, Dean T, Rowlandson P, Gant C, Grundy J, Fitzgerald C, Stevenson J. The effects of a double blind, placebo controlled, artificial food colourings and benzoate preservative challenge on hyperactivity in a general population sample of preschool children. Archives of disease in childhood 2004;89(6):506-11
https://pubmed.ncbi.nlm.nih.gov/15155391[13] Bhatia J, Greer F, . Use of soy protein-based formulas in infant feeding. Pediatrics 2008;121(5):1062-8
http://dx.doi.org/10.1542/peds.2008-0564 https://pubmed.ncbi.nlm.nih.gov/18450914[14] Bianchi ML, Bardella MT. Bone and celiac disease. Calcified tissue international 2002;71(6):465-71
https://pubmed.ncbi.nlm.nih.gov/12232681[15] Bock SA. Prospective appraisal of complaints of adverse reactions to foods in children during the first 3 years of life. Pediatrics 1987;79(5):683-8
https://pubmed.ncbi.nlm.nih.gov/3575022[16] Bock SA, Muñoz-Furlong A, Sampson HA. Fatalities due to anaphylactic reactions to foods. The Journal of allergy and clinical immunology 2001;107(1):191-3
https://pubmed.ncbi.nlm.nih.gov/11150011[17] Bourgey M, Calcagno G, Tinto N, Gennarelli D, Margaritte-Jeannin P, Greco L, Limongelli MG, Esposito O, Marano C, Troncone R, Spampanato A, Clerget-Darpoux F, Sacchetti L. HLA related genetic risk for coeliac disease. Gut 2007;56(8):1054-9
https://pubmed.ncbi.nlm.nih.gov/17344279[18] Boyce JA, Assa'a A, Burks AW, Jones SM, Sampson HA, Wood RA, Plaut M, Cooper SF, Fenton MJ, Arshad SH, Bahna SL, Beck LA, Byrd-Bredbenner C, Camargo CA, Eichenfield L, Furuta GT, Hanifin JM, Jones C, Kraft M, Levy BD, Lieberman P, Luccioli S, McCall KM, Schneider LC, Simon RA, Simons FER, Teach SJ, Yawn BP, Schwaninger JM, . Guidelines for the diagnosis and management of food allergy in the United States: summary of the NIAID-Sponsored Expert Panel Report. Nutrition (Burbank, Los Angeles County, Calif.) 2011;27(2):253-67
http://dx.doi.org/10.1016/j.nut.2010.12.001 https://pubmed.ncbi.nlm.nih.gov/21215925[19] , Boyce JA, Assa'ad A, Burks AW, Jones SM, Sampson HA, Wood RA, Plaut M, Cooper SF, Fenton MJ, Arshad SH, Bahna SL, Beck LA, Byrd-Bredbenner C, Camargo CA, Eichenfield L, Furuta GT, Hanifin JM, Jones C, Kraft M, Levy BD, Lieberman P, Luccioli S, McCall KM, Schneider LC, Simon RA, Simons FER, Teach SJ, Yawn BP, Schwaninger JM. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID-sponsored expert panel. The Journal of allergy and clinical immunology 2010;126(6 Suppl):S1-58
http://dx.doi.org/10.1016/j.jaci.2010.10.007 https://pubmed.ncbi.nlm.nih.gov/21134576[20] Suchy FJ, Brannon PM, Carpenter TO, Fernandez JR, Gilsanz V, Gould JB, Hall K, Hui SL, Lupton J, Mennella J, Miller NJ, Osganian SK, Sellmeyer DE, Wolf MA. NIH consensus development conference statement: Lactose intolerance and health. NIH consensus and state-of-the-science statements 2010;27(2):1-27
https://pubmed.ncbi.nlm.nih.gov/20186234[21] Brousse N, Meijer JWR. Malignant complications of coeliac disease. Best practice & research. Clinical gastroenterology 2005;19(3):401-12
https://pubmed.ncbi.nlm.nih.gov/15925845[22] Burks AW, Jones SM, Boyce JA, Sicherer SH, Wood RA, Assa'ad A, Sampson HA. NIAID-sponsored 2010 guidelines for managing food allergy: applications in the pediatric population. Pediatrics 2011;128(5):955-65
http://dx.doi.org/10.1542/peds.2011-0539 https://pubmed.ncbi.nlm.nih.gov/21987705[23] Burks W, Jones SM, Berseth CL, Harris C, Sampson HA, Scalabrin DMF. Hypoallergenicity and effects on growth and tolerance of a new amino acid-based formula with docosahexaenoic acid and arachidonic acid. The Journal of pediatrics 2008;153(2):266-71
http://dx.doi.org/10.1016/j.jpeds.2008.02.043 https://pubmed.ncbi.nlm.nih.gov/18534230[24] Businco L, Dreborg S, Einarsson R, Giampietro PG, Høst A, Keller KM, Strobel S, Wahn U, Björkstén B, Kjellman MN. Hydrolysed cow's milk formulae. Allergenicity and use in treatment and prevention. An ESPACI position paper. European Society of Pediatric Allergy and Clinical Immunology. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1993;4(3):101-11
https://pubmed.ncbi.nlm.nih.gov/8220797[25] Byrne AM, Malka-Rais J, Burks AW, Fleischer DM. How do we know when peanut and tree nut allergy have resolved, and how do we keep it resolved? Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2010;40(9):1303-11
http://dx.doi.org/10.1111/j.1365-2222.2010.03554.x https://pubmed.ncbi.nlm.nih.gov/20645999[26] Caffarelli C, Plebani A, Poiesi C, Petroccione T, Spattini A, Cavagni G. Determination of allergenicity to three cow's milk hydrolysates and an amino acid-derived formula in children with cow's milk allergy. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2002;32(1):74-9
https://pubmed.ncbi.nlm.nih.gov/12002741[27] Carter CM, Urbanowicz M, Hemsley R, Mantilla L, Strobel S, Graham PJ, Taylor E. Effects of a few food diet in attention deficit disorder. Archives of disease in childhood 1993;69(5):564-8
https://pubmed.ncbi.nlm.nih.gov/8257176[28] Cash BD, Schoenfeld P, Chey WD. The utility of diagnostic tests in irritable bowel syndrome patients: a systematic review. The American journal of gastroenterology 2002;97(11):2812-9
https://pubmed.ncbi.nlm.nih.gov/12425553[29] Chafen JJS, Newberry SJ, Riedl MA, Bravata DM, Maglione M, Suttorp MJ, Sundaram V, Paige NM, Towfigh A, Hulley BJ, Shekelle PG. Diagnosing and managing common food allergies: a systematic review. JAMA 2010;303(18):1848-56
http://dx.doi.org/10.1001/jama.2010.582 https://pubmed.ncbi.nlm.nih.gov/20460624[30] Csizmadia CG, Mearin ML, von Blomberg BM, Brand R, Verloove-Vanhorick SP. An iceberg of childhood coeliac disease in the Netherlands. Lancet (London, England) 1999;353(9155):813-4
https://pubmed.ncbi.nlm.nih.gov/10459972[31] de Graaff LCG, Smit JWA, Radder JK. Prevalence and clinical significance of organ-specific autoantibodies in type 1 diabetes mellitus. The Netherlands journal of medicine 2007;65(7):235-47
https://pubmed.ncbi.nlm.nih.gov/17656810[32] de Jong MH, Scharp-Van Der Linden VTM, Aalberse R, Heymans HSA, Brunekreef B. The effect of brief neonatal exposure to cows' milk on atopic symptoms up to age 5. Archives of disease in childhood 2002;86(5):365-9
https://pubmed.ncbi.nlm.nih.gov/11970933[33] de Jong MH, Scharp-van der Linden VT, Aalberse RC, Oosting J, Tijssen JG, de Groot CJ. Randomised controlled trial of brief neonatal exposure to cows' milk on the development of atopy. Archives of disease in childhood 1998;79(2):126-30
https://pubmed.ncbi.nlm.nih.gov/9797592[34] de Vrese M, Schrezenmeir J. Probiotics, prebiotics, and synbiotics. Advances in biochemical engineering/biotechnology 2008;111():1-66
http://dx.doi.org/10.1007/10_2008_097 https://pubmed.ncbi.nlm.nih.gov/18461293[35] Dengate S, Ruben A. Controlled trial of cumulative behavioural effects of a common bread preservative. Journal of paediatrics and child health 2002;38(4):373-6
https://pubmed.ncbi.nlm.nih.gov/12173999[36] Du Toit G, Katz Y, Sasieni P, Mesher D, Maleki SJ, Fisher HR, Fox AT, Turcanu V, Amir T, Zadik-Mnuhin G, Cohen A, Livne I, Lack G. Early consumption of peanuts in infancy is associated with a low prevalence of peanut allergy. The Journal of allergy and clinical immunology 2008;122(5):984-91
http://dx.doi.org/10.1016/j.jaci.2008.08.039 https://pubmed.ncbi.nlm.nih.gov/19000582[37] du Toit G, Meyer R, Shah N, Heine RG, Thomson MA, Lack G, Fox AT. Identifying and managing cow's milk protein allergy. Archives of disease in childhood. Education and practice edition 2010;95(5):134-44
http://dx.doi.org/10.1136/adc.2007.118018 https://pubmed.ncbi.nlm.nih.gov/20688848[38] Egger J, Carter CM, Graham PJ, Gumley D, Soothill JF. Controlled trial of oligoantigenic treatment in the hyperkinetic syndrome. Lancet (London, England) 1985;1(8428):540-5
https://pubmed.ncbi.nlm.nih.gov/2857900[39] Fälth-Magnusson K, Franzén L, Jansson G, Laurin P, Stenhammar L. Infant feeding history shows distinct differences between Swedish celiac and reference children. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1996;7(1):1-5
https://pubmed.ncbi.nlm.nih.gov/8792377[40] Feingold BF. Hyperkinesis and learning disabilities linked to artificial food flavors and colors. The American journal of nursing 1975;75(5):797-803
https://pubmed.ncbi.nlm.nih.gov/1039267[41] Filipiak B, Zutavern A, Koletzko S, von Berg A, Brockow I, Grübl A, Berdel D, Reinhardt D, Bauer CP, Wichmann H-E, Heinrich J, . Solid food introduction in relation to eczema: results from a four-year prospective birth cohort study. The Journal of pediatrics 2007;151(4):352-8
https://pubmed.ncbi.nlm.nih.gov/17889067[42] Fiocchi A, Brozek J, Schünemann H, Bahna SL, von Berg A, Beyer K, Bozzola M, Bradsher J, Compalati E, Ebisawa M, Guzmán MA, Li H, Heine RG, Keith P, Lack G, Landi M, Martelli A, Rancé F, Sampson H, Stein A, Terracciano L, Vieths S, . World Allergy Organization (WAO) Diagnosis and Rationale for Action against Cow's Milk Allergy (DRACMA) Guidelines. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2010;21 Suppl 21():1-125
http://dx.doi.org/10.1111/j.1399-3038.2010.01068.x https://pubmed.ncbi.nlm.nih.gov/20618740[43] Ford AC, Chey WD, Talley NJ, Malhotra A, Spiegel BMR, Moayyedi P. Yield of diagnostic tests for celiac disease in individuals with symptoms suggestive of irritable bowel syndrome: systematic review and meta-analysis. Archives of internal medicine 2009;169(7):651-8
http://dx.doi.org/10.1001/archinternmed.2009.22 https://pubmed.ncbi.nlm.nih.gov/19364994[44] Ford AC, Ching E, Moayyedi P. Meta-analysis: yield of diagnostic tests for coeliac disease in dyspepsia. Alimentary pharmacology & therapeutics 2009;30(1):28-36
http://dx.doi.org/10.1111/j.1365-2036.2009.04008.x https://pubmed.ncbi.nlm.nih.gov/19416130[45] Gijsbers CFM, Kneepkens CMF, Büller HA. Lactose and fructose malabsorption in children with recurrent abdominal pain: results of double-blinded testing. Acta paediatrica (Oslo, Norway : 1992) 2012;101(9):e411-5
http://dx.doi.org/10.1111/j.1651-2227.2012.02721.x https://pubmed.ncbi.nlm.nih.gov/22578243[46] Giuca MR, Cei G, Gigli F, Gandini P. Oral signs in the diagnosis of celiac disease: review of the literature. Minerva stomatologica 2010;59(1-2):33-43
https://pubmed.ncbi.nlm.nih.gov/20212408[47] Goddard CJR, Gillett HR. Complications of coeliac disease: are all patients at risk? Postgraduate medical journal 2006;82(973):705-12
https://pubmed.ncbi.nlm.nih.gov/17099088[48] Gravholt CH. Clinical practice in Turner syndrome. Nature clinical practice. Endocrinology & metabolism 2005;1(1):41-52
https://pubmed.ncbi.nlm.nih.gov/16929365[49] Greco L, Auricchio S, Mayer M, Grimaldi M. Case control study on nutritional risk factors in celiac disease. Journal of pediatric gastroenterology and nutrition 1988;7(3):395-9
https://pubmed.ncbi.nlm.nih.gov/3385552[50] Grossman G. Neurological complications of coeliac disease: what is the evidence? Practical neurology 2008;8(2):77-89
http://dx.doi.org/10.1136/jnnp.2007.139717 https://pubmed.ncbi.nlm.nih.gov/18344378[51] Gutierrez-Achury J, Coutinho de Almeida R, Wijmenga C. Shared genetics in coeliac disease and other immune-mediated diseases. Journal of internal medicine 2011;269(6):591-603
http://dx.doi.org/10.1111/j.1365-2796.2011.02375.x https://pubmed.ncbi.nlm.nih.gov/21401738[52] Haines ML, Anderson RP, Gibson PR. Systematic review: The evidence base for long-term management of coeliac disease. Alimentary pharmacology & therapeutics 2008;28(9):1042-66
http://dx.doi.org/10.1111/j.1365-2036.2008.03820.x https://pubmed.ncbi.nlm.nih.gov/18671779[53] Halmerbauer G, Gartner C, Schier M, Arshad H, Dean T, Koller DY, Karmaus W, Kuehr J, Forster J, Urbanek R, Frischer T, . Study on the prevention of allergy in Children in Europe (SPACE): allergic sensitization in children at 1 year of age in a controlled trial of allergen avoidance from birth. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2002;13(s15):47-54
https://pubmed.ncbi.nlm.nih.gov/12688625[54] Hattevig G, Kjellman B, Sigurs N, Björkstén B, Kjellman NI. Effect of maternal avoidance of eggs, cow's milk and fish during lactation upon allergic manifestations in infants. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 1989;19(1):27-32
https://pubmed.ncbi.nlm.nih.gov/2702510[55] Hays T, Wood RA. A systematic review of the role of hydrolyzed infant formulas in allergy prevention. Archives of pediatrics & adolescent medicine 2005;159(9):810-6
https://pubmed.ncbi.nlm.nih.gov/16143739[56] Heyman MB, . Lactose intolerance in infants, children, and adolescents. Pediatrics 2006;118(3):1279-86
https://pubmed.ncbi.nlm.nih.gov/16951027[57] Hill DJ, Murch SH, Rafferty K, Wallis P, Green CJ. The efficacy of amino acid-based formulas in relieving the symptoms of cow's milk allergy: a systematic review. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2007;37(6):808-22
https://pubmed.ncbi.nlm.nih.gov/17517094[58] Hill ID, Dirks MH, Liptak GS, Colletti RB, Fasano A, Guandalini S, Hoffenberg EJ, Horvath K, Murray JA, Pivor M, Seidman EG, . Guideline for the diagnosis and treatment of celiac disease in children: recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. Journal of pediatric gastroenterology and nutrition 2005;40(1):1-19
https://pubmed.ncbi.nlm.nih.gov/15625418[59] Hogen Esch CE, Rosén A, Auricchio R, Romanos J, Chmielewska A, Putter H, Ivarsson A, Szajewska H, Koning F, Wijmenga C, Troncone R, Mearin ML, . The PreventCD Study design: towards new strategies for the prevention of coeliac disease. European journal of gastroenterology & hepatology 2010;22(12):1424-30
http://dx.doi.org/10.1097/MEG.0b013e32833fe9ae https://pubmed.ncbi.nlm.nih.gov/21389794[60] Husby S, Koletzko S, Korponay-Szabó IR, Mearin ML, Phillips A, Shamir R, Troncone R, Giersiepen K, Branski D, Catassi C, Lelgeman M, Mäki M, Ribes-Koninckx C, Ventura A, Zimmer KP, , , . European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. Journal of pediatric gastroenterology and nutrition 2012;54(1):136-60
http://dx.doi.org/10.1097/MPG.0b013e31821a23d0 https://pubmed.ncbi.nlm.nih.gov/22197856[61] Huurre A, Laitinen K, Rautava S, Korkeamäki M, Isolauri E. Impact of maternal atopy and probiotic supplementation during pregnancy on infant sensitization: a double-blind placebo-controlled study. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2008;38(8):1342-8
http://dx.doi.org/10.1111/j.1365-2222.2008.03008.x https://pubmed.ncbi.nlm.nih.gov/18477013[62] Iacono G, Carroccio A, Cavataio F, Montalto G, Cantarero MD, Notarbartolo A. Chronic constipation as a symptom of cow milk allergy. The Journal of pediatrics 1995;126(1):34-9
https://pubmed.ncbi.nlm.nih.gov/7815220[63] Ingen-Housz-Oro S. [Dermatitis herpetiformis: a review]. Annales de dermatologie et de venereologie 2011;138(3):221-7
http://dx.doi.org/10.1016/j.annder.2011.01.005 https://pubmed.ncbi.nlm.nih.gov/21397152[64] Isolauri E, Sütas Y, Mäkinen-Kiljunen S, Oja SS, Isosomppi R, Turjanmaa K. Efficacy and safety of hydrolyzed cow milk and amino acid-derived formulas in infants with cow milk allergy. The Journal of pediatrics 1995;127(4):550-7
https://pubmed.ncbi.nlm.nih.gov/7562275[65] Ivarsson A, Hernell O, Stenlund H, Persson LA. Breast-feeding protects against celiac disease. The American journal of clinical nutrition 2002;75(5):914-21
https://pubmed.ncbi.nlm.nih.gov/11976167[66] Jadad AR, Moore RA, Carroll D, Jenkinson C, Reynolds DJ, Gavaghan DJ, McQuay HJ. Assessing the quality of reports of randomized clinical trials: is blinding necessary? Controlled clinical trials 1996;17(1):1-12
https://pubmed.ncbi.nlm.nih.gov/8721797[67] James JM, Bernhisel-Broadbent J, Sampson HA. Respiratory reactions provoked by double-blind food challenges in children. American journal of respiratory and critical care medicine 1994;149(1):59-64
https://pubmed.ncbi.nlm.nih.gov/8111598[68] Järvelä IE. Molecular genetics of adult-type hypolactasia. Annals of medicine 2005;37(3):179-85
https://pubmed.ncbi.nlm.nih.gov/16019716[69] Järvinen KM, Chatchatee P. Mammalian milk allergy: clinical suspicion, cross-reactivities and diagnosis. Current opinion in allergy and clinical immunology 2009;9(3):251-8
http://dx.doi.org/10.1097/ACI.0b013e32832b3f33 https://pubmed.ncbi.nlm.nih.gov/19412090[70] Jellema P, Schellevis FG, van der Windt DAWM, Kneepkens CMF, van der Horst HE. Lactose malabsorption and intolerance: a systematic review on the diagnostic value of gastrointestinal symptoms and self-reported milk intolerance. QJM : monthly journal of the Association of Physicians 2010;103(8):555-72
http://dx.doi.org/10.1093/qjmed/hcq082 https://pubmed.ncbi.nlm.nih.gov/20522486[71] Kajosaari M. Atopy prevention in childhood: the role of diet. Prospective 5-year follow-up of high-risk infants with six months exclusive breastfeeding and solid food elimination. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1994;5(6 Suppl):26-8
https://pubmed.ncbi.nlm.nih.gov/7728225[72] Katz Y, Rajuan N, Goldberg MR, Eisenberg E, Heyman E, Cohen A, Leshno M. Early exposure to cow's milk protein is protective against IgE-mediated cow's milk protein allergy. The Journal of allergy and clinical immunology 2010;126(1):77-82.e1
http://dx.doi.org/10.1016/j.jaci.2010.04.020 https://pubmed.ncbi.nlm.nih.gov/20541249[73] Kerkhof M, Wijga A, Smit HA, de Jongste JC, Aalberse RC, Brunekreef B, Gerritsen J, Postma DS, . The effect of prenatal exposure on total IgE at birth and sensitization at twelve months and four years of age: The PIAMA study. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2005;16(1):10-8
https://pubmed.ncbi.nlm.nih.gov/15693906[74] Klemola T, Vanto T, Juntunen-Backman K, Kalimo K, Korpela R, Varjonen E. Allergy to soy formula and to extensively hydrolyzed whey formula in infants with cow's milk allergy: a prospective, randomized study with a follow-up to the age of 2 years. The Journal of pediatrics 2002;140(2):219-24
https://pubmed.ncbi.nlm.nih.gov/11865274[75] Klemola T, Kalimo K, Poussa T, Juntunen-Backman K, Korpela R, Valovirta E, Vanto T. Feeding a soy formula to children with cow's milk allergy: the development of immunoglobulin E-mediated allergy to soy and peanuts. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2005;16(8):641-6
https://pubmed.ncbi.nlm.nih.gov/16343085[76] Kneepkens CMF, Meijer Y. Clinical practice. Diagnosis and treatment of cow's milk allergy. European journal of pediatrics 2009;168(8):891-6
http://dx.doi.org/10.1007/s00431-009-0955-7 https://pubmed.ncbi.nlm.nih.gov/19271238[77] Kuitunen M, Kukkonen K, Juntunen-Backman K, Korpela R, Poussa T, Tuure T, Haahtela T, Savilahti E. Probiotics prevent IgE-associated allergy until age 5 years in cesarean-delivered children but not in the total cohort. The Journal of allergy and clinical immunology 2009;123(2):335-41
http://dx.doi.org/10.1016/j.jaci.2008.11.019 https://pubmed.ncbi.nlm.nih.gov/19135235[78] Kukkonen K, Savilahti E, Haahtela T, Juntunen-Backman K, Korpela R, Poussa T, Tuure T, Kuitunen M. Probiotics and prebiotic galacto-oligosaccharides in the prevention of allergic diseases: a randomized, double-blind, placebo-controlled trial. The Journal of allergy and clinical immunology 2007;119(1):192-8
https://pubmed.ncbi.nlm.nih.gov/17208601[79] Lack G. Clinical practice. Food allergy. The New England journal of medicine 2008;359(12):1252-60
http://dx.doi.org/10.1056/NEJMcp0800871 https://pubmed.ncbi.nlm.nih.gov/18799559[80] Lannerö E, Wickman M, van Hage M, Bergström A, Pershagen G, Nordvall L. Exposure to environmental tobacco smoke and sensitisation in children. Thorax 2008;63(2):172-6
https://pubmed.ncbi.nlm.nih.gov/18089631[81] Laubereau B, Brockow I, Zirngibl A, Koletzko S, Gruebl A, von Berg A, Filipiak-Pittroff B, Berdel D, Bauer CP, Reinhardt D, Heinrich J, Wichmann H-E, . Effect of breast-feeding on the development of atopic dermatitis during the first 3 years of life--results from the GINI-birth cohort study. The Journal of pediatrics 2004;144(5):602-7
https://pubmed.ncbi.nlm.nih.gov/15126993[82] Lindfors AT, Danielsson L, Enocksson E, Johansson SG, Westin S. Allergic symptoms up to 4-6 years of age in children given cow milk neonatally. A prospective study. Allergy 1992;47(3):207-11
https://pubmed.ncbi.nlm.nih.gov/1510232[83] McCann D, Barrett A, Cooper A, Crumpler D, Dalen L, Grimshaw K, Kitchin E, Lok K, Porteous L, Prince E, Sonuga-Barke E, Warner JO, Stevenson J. Food additives and hyperactive behaviour in 3-year-old and 8/9-year-old children in the community: a randomised, double-blinded, placebo-controlled trial. Lancet (London, England) 2007;370(9598):1560-7
https://pubmed.ncbi.nlm.nih.gov/17825405[84] McCarver G, Bhatia J, Chambers C, Clarke R, Etzel R, Foster W, Hoyer P, Leeder JS, Peters JM, Rissman E, Rybak M, Sherman C, Toppari J, Turner K. NTP-CERHR expert panel report on the developmental toxicity of soy infant formula. Birth defects research. Part B, Developmental and reproductive toxicology 2011;92(5):421-68
http://dx.doi.org/10.1002/bdrb.20314 https://pubmed.ncbi.nlm.nih.gov/21948615[85] Mennella JA, Beauchamp GK. Flavor experiences during formula feeding are related to preferences during childhood. Early human development 2002;68(2):71-82
https://pubmed.ncbi.nlm.nih.gov/12113993[86] Mirzaagha F, Azali SH, Islami F, Zamani F, Khalilipour E, Khatibian M, Malekzadeh R. Coeliac disease in autoimmune liver disease: a cross-sectional study and a systematic review. Digestive and liver disease : official journal of the Italian Society of Gastroenterology and the Italian Association for the Study of the Liver 2010;42(9):620-3
http://dx.doi.org/10.1016/j.dld.2010.02.006 https://pubmed.ncbi.nlm.nih.gov/20236872[87] Moro G, Arslanoglu S, Stahl B, Jelinek J, Wahn U, Boehm G. A mixture of prebiotic oligosaccharides reduces the incidence of atopic dermatitis during the first six months of age. Archives of disease in childhood 2006;91(10):814-9
https://pubmed.ncbi.nlm.nih.gov/16873437[88] Muraro A, Roberts G, Clark A, Eigenmann PA, Halken S, Lack G, Moneret-Vautrin A, Niggemann B, Rancé F, . The management of anaphylaxis in childhood: position paper of the European academy of allergology and clinical immunology. Allergy 2007;62(8):857-71
https://pubmed.ncbi.nlm.nih.gov/17590200[89] Niggemann B, Binder C, Dupont C, Hadji S, Arvola T, Isolauri E. Prospective, controlled, multi-center study on the effect of an amino-acid-based formula in infants with cow's milk allergy/intolerance and atopic dermatitis. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2001;12(2):78-82
https://pubmed.ncbi.nlm.nih.gov/11338290[90] Niggemann B, von Berg A, Bollrath C, Berdel D, Schauer U, Rieger C, Haschke-Becher E, Wahn U. Safety and efficacy of a new extensively hydrolyzed formula for infants with cow's milk protein allergy. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2008;19(4):348-54
http://dx.doi.org/10.1111/j.1399-3038.2007.00653.x https://pubmed.ncbi.nlm.nih.gov/18167160[91] Nova E, Pozo T, Sanz Y, Marcos A. Dietary strategies of immunomodulation in infants at risk for celiac disease. The Proceedings of the Nutrition Society 2010;69(3):347-53
http://dx.doi.org/10.1017/S0029665110001825 https://pubmed.ncbi.nlm.nih.gov/20579407[92] Nowak-Wegrzyn A, Assa'ad AH, Bahna SL, Bock SA, Sicherer SH, Teuber SS, . Work Group report: oral food challenge testing. The Journal of allergy and clinical immunology 2009;123(6 Suppl):S365-83
http://dx.doi.org/10.1016/j.jaci.2009.03.042 https://pubmed.ncbi.nlm.nih.gov/19500710[93] Nowak-Wegrzyn A, Fiocchi A. Rare, medium, or well done? The effect of heating and food matrix on food protein allergenicity. Current opinion in allergy and clinical immunology 2009;9(3):234-7
http://dx.doi.org/10.1097/ACI.0b013e32832b88e7 https://pubmed.ncbi.nlm.nih.gov/19444093[94] Nwaru BI, Erkkola M, Ahonen S, Kaila M, Haapala A-M, Kronberg-Kippilä C, Salmelin R, Veijola R, Ilonen J, Simell O, Knip M, Virtanen SM. Age at the introduction of solid foods during the first year and allergic sensitization at age 5 years. Pediatrics 2010;125(1):50-9
http://dx.doi.org/10.1542/peds.2009-0813 https://pubmed.ncbi.nlm.nih.gov/19969611[95] Odelram H, Vanto T, Jacobsen L, Kjellman NI. Whey hydrolysate compared with cow's milk-based formula for weaning at about 6 months of age in high allergy-risk infants: effects on atopic disease and sensitization. Allergy 1996;51(3):192-5
https://pubmed.ncbi.nlm.nih.gov/8781676[96] Osborn DA, Sinn J. Formulas containing hydrolysed protein for prevention of allergy and food intolerance in infants. The Cochrane database of systematic reviews 2003
https://pubmed.ncbi.nlm.nih.gov/14583987[97] Osborn DA, Sinn J. Soy formula for prevention of allergy and food intolerance in infants. The Cochrane database of systematic reviews 2006;2006(4):CD003741
https://pubmed.ncbi.nlm.nih.gov/17054183[98] Osborn DA, Sinn JK. Prebiotics in infants for prevention of allergic disease and food hypersensitivity. The Cochrane database of systematic reviews 2007
https://pubmed.ncbi.nlm.nih.gov/17943911[99] Pastore L, Carroccio A, Compilato D, Panzarella V, Serpico R, Lo Muzio L. Oral manifestations of celiac disease. Journal of clinical gastroenterology 2008;42(3):224-32
http://dx.doi.org/10.1097/MCG.0b013e318074dd98 https://pubmed.ncbi.nlm.nih.gov/18223505[100] Pelsser LM, Frankena K, Toorman J, Savelkoul HF, Dubois AE, Pereira RR, Haagen TA, Rommelse NN, Buitelaar JK. Effects of a restricted elimination diet on the behaviour of children with attention-deficit hyperactivity disorder (INCA study): a randomised controlled trial. Lancet (London, England) 2011;377(9764):494-503
http://dx.doi.org/10.1016/S0140-6736(10)62227-1 https://pubmed.ncbi.nlm.nih.gov/21296237[101] Pengiran Tengah DSNA, Wills AJ, Holmes GKT. Neurological complications of coeliac disease. Postgraduate medical journal 2002;78(921):393-8
https://pubmed.ncbi.nlm.nih.gov/12151653[102] Perry TT, Matsui EC, Conover-Walker MK, Wood RA. Risk of oral food challenges. The Journal of allergy and clinical immunology 2004;114(5):1164-8
https://pubmed.ncbi.nlm.nih.gov/15536426[103] Peters U, Schneeweiss S, Trautwein EA, Erbersdobler HF. A case-control study of the effect of infant feeding on celiac disease. Annals of nutrition & metabolism 2001;45(4):135-42
https://pubmed.ncbi.nlm.nih.gov/11463995[104] Pumphrey RSH. Fatal anaphylaxis in the UK, 1992-2001. Novartis Foundation symposium 2004;257():116-28; discussion 128-32, 157-60, 276-85
https://pubmed.ncbi.nlm.nih.gov/15025395[105] Pumphrey RSH, Gowland MH. Further fatal allergic reactions to food in the United Kingdom, 1999-2006. The Journal of allergy and clinical immunology 2007;119(4):1018-9
https://pubmed.ncbi.nlm.nih.gov/17349682[106] Rancé F, Kanny G, Dutau G, Moneret-Vautrin DA. Food hypersensitivity in children: clinical aspects and distribution of allergens. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1999;10(1):33-8
https://pubmed.ncbi.nlm.nih.gov/10410915[107] Rautava S, Kalliomäki M, Isolauri E. Probiotics during pregnancy and breast-feeding might confer immunomodulatory protection against atopic disease in the infant. The Journal of allergy and clinical immunology 2002;109(1):119-21
https://pubmed.ncbi.nlm.nih.gov/11799376[108] Roizen NJ, Patterson D. Down's syndrome. Lancet (London, England) 2003;361(9365):1281-9
https://pubmed.ncbi.nlm.nih.gov/12699967[109] Sainsbury A, Sanders DS, Ford AC. Meta-analysis: Coeliac disease and hypertransaminasaemia. Alimentary pharmacology & therapeutics 2011;34(1):33-40
http://dx.doi.org/10.1111/j.1365-2036.2011.04685.x https://pubmed.ncbi.nlm.nih.gov/21545472[110] Salvatore S, Vandenplas Y. Gastroesophageal reflux and cow milk allergy: is there a link? Pediatrics 2002;110(5):972-84
https://pubmed.ncbi.nlm.nih.gov/12415039[111] Sampson HA, James JM, Bernhisel-Broadbent J. Safety of an amino acid-derived infant formula in children allergic to cow milk. Pediatrics 1992;90(3):463-5
https://pubmed.ncbi.nlm.nih.gov/1518709[112] Sattar N, Lazare F, Kacer M, Aguayo-Figueroa L, Desikan V, Garcia M, Lane A, Chawla A, Wilson T. Celiac disease in children, adolescents, and young adults with autoimmune thyroid disease. The Journal of pediatrics 2011;158(2):272-5.e1
http://dx.doi.org/10.1016/j.jpeds.2010.08.050 https://pubmed.ncbi.nlm.nih.gov/20961564[113] Sausenthaler S, Heinrich J, Koletzko S, . Early diet and the risk of allergy: what can we learn from the prospective birth cohort studies GINIplus and LISAplus? The American journal of clinical nutrition 2011;94(6 Suppl):2012S-2017S
http://dx.doi.org/10.3945/ajcn.110.001180 https://pubmed.ncbi.nlm.nih.gov/21543544[114] Savaiano DA, Boushey CJ, McCabe GP. Lactose intolerance symptoms assessed by meta-analysis: a grain of truth that leads to exaggeration. The Journal of nutrition 2006;136(4):1107-13
https://pubmed.ncbi.nlm.nih.gov/16549489[115] Schab DW, Trinh N-HT. Do artificial food colors promote hyperactivity in children with hyperactive syndromes? A meta-analysis of double-blind placebo-controlled trials. Journal of developmental and behavioral pediatrics : JDBP 2004;25(6):423-34
https://pubmed.ncbi.nlm.nih.gov/15613992[116] Schoetzau A, Filipiak-Pittroff B, Franke K, Koletzko S, Von Berg A, Gruebl A, Bauer CP, Berdel D, Reinhardt D, Wichmann H-E, . Effect of exclusive breast-feeding and early solid food avoidance on the incidence of atopic dermatitis in high-risk infants at 1 year of age. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2002;13(4):234-42
https://pubmed.ncbi.nlm.nih.gov/12390439[117] Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH, . Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ (Clinical research ed.) 2008;336(7653):1106-10
http://dx.doi.org/10.1136/bmj.39500.677199.AE https://pubmed.ncbi.nlm.nih.gov/18483053[118] Shaukat A, Levitt MD, Taylor BC, MacDonald R, Shamliyan TA, Kane RL, Wilt TJ. Systematic review: effective management strategies for lactose intolerance. Annals of internal medicine 2010;152(12):797-803
http://dx.doi.org/10.7326/0003-4819-152-12-201006150-00241 https://pubmed.ncbi.nlm.nih.gov/20404262[119] Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, Porter AC, Tugwell P, Moher D, Bouter LM. Development of AMSTAR: a measurement tool to assess the methodological quality of systematic reviews. BMC medical research methodology 2007;7():10
https://pubmed.ncbi.nlm.nih.gov/17302989[120] Sigurs N, Hattevig G, Kjellman B. Maternal avoidance of eggs, cow's milk, and fish during lactation: effect on allergic manifestations, skin-prick tests, and specific IgE antibodies in children at age 4 years. Pediatrics 1992;89(4 Pt 2):735-9
https://pubmed.ncbi.nlm.nih.gov/1557270[121] Silano M, Agostoni C, Guandalini S. Effect of the timing of gluten introduction on the development of celiac disease. World journal of gastroenterology 2010;16(16):1939-42
https://pubmed.ncbi.nlm.nih.gov/20419830[122] Snijders BEP, Thijs C, van Ree R, van den Brandt PA. Age at first introduction of cow milk products and other food products in relation to infant atopic manifestations in the first 2 years of life: the KOALA Birth Cohort Study. Pediatrics 2008;122(1):e115-22
http://dx.doi.org/10.1542/peds.2007-1651 https://pubmed.ncbi.nlm.nih.gov/18595956[123] Stallings VA. Calcium and bone health in children: a review. American journal of therapeutics 1997;4(7-8):259-73
https://pubmed.ncbi.nlm.nih.gov/10423619[124] Steens RFR, Csizmadia CGDS, George EK, Ninaber MK, Hira Sing RA, Mearin ML. A national prospective study on childhood celiac disease in the Netherlands 1993-2000: an increasing recognition and a changing clinical picture. The Journal of pediatrics 2005;147(2):239-43
https://pubmed.ncbi.nlm.nih.gov/16126057[125] Syrigou EI, Pitsios C, Panagiotou I, Chouliaras G, Kitsiou S, Kanariou M, Roma-Giannikou E. Food allergy-related paediatric constipation: the usefulness of atopy patch test. European journal of pediatrics 2011;170(9):1173-8
http://dx.doi.org/10.1007/s00431-011-1417-6 https://pubmed.ncbi.nlm.nih.gov/21347849[126] Szajewska H, Mrukowicz JZ, Stoińska B, Prochowska A. Extensively and partially hydrolysed preterm formulas in the prevention of allergic diseases in preterm infants: a randomized, double-blind trial. Acta paediatrica (Oslo, Norway : 1992) 2004;93(9):1159-65
https://pubmed.ncbi.nlm.nih.gov/15384877[127] Szajewska H, Chmielewska A, Pieścik-Lech M, Ivarsson A, Kolacek S, Koletzko S, Mearin ML, Shamir R, Auricchio R, Troncone R, . Systematic review: early infant feeding and the prevention of coeliac disease. Alimentary pharmacology & therapeutics 2012;36(7):607-18
http://dx.doi.org/10.1111/apt.12023 https://pubmed.ncbi.nlm.nih.gov/22905651[128] Szilagyi A, Nathwani U, Vinokuroff C, Correa JA, Shrier I. The effect of lactose maldigestion on the relationship between dairy food intake and colorectal cancer: a systematic review. Nutrition and cancer 2006;55(2):141-50
https://pubmed.ncbi.nlm.nih.gov/17044768[129] Terracciano L, Bouygue GR, Sarratud T, Veglia F, Martelli A, Fiocchi A. Impact of dietary regimen on the duration of cow's milk allergy: a random allocation study. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2010;40(4):637-42
http://dx.doi.org/10.1111/j.1365-2222.2009.03427.x https://pubmed.ncbi.nlm.nih.gov/20067480[130] Tromp IIM, Kiefte-de Jong JC, Lebon A, Renders CM, Jaddoe VWV, Hofman A, de Jongste JC, Moll HA. The introduction of allergenic foods and the development of reported wheezing and eczema in childhood: the Generation R study. Archives of pediatrics & adolescent medicine 2011;165(10):933-8
http://dx.doi.org/10.1001/archpediatrics.2011.93 https://pubmed.ncbi.nlm.nih.gov/21646571[131] van der Aa LB, Heymans HSA, van Aalderen WMC, Sprikkelman AB. Probiotics and prebiotics in atopic dermatitis: review of the theoretical background and clinical evidence. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2010;21(2 Pt 2):e355-67
http://dx.doi.org/10.1111/j.1399-3038.2009.00915.x https://pubmed.ncbi.nlm.nih.gov/19573143[132] van der Windt DAWM, Jellema P, Mulder CJ, Kneepkens CMF, van der Horst HE. Diagnostic testing for celiac disease among patients with abdominal symptoms: a systematic review. JAMA 2010;303(17):1738-46
http://dx.doi.org/10.1001/jama.2010.549 https://pubmed.ncbi.nlm.nih.gov/20442390[133] Vanderhoof JA. Hypoallergenicity and effects on growth and tolerance of a new amino acid-based formula with DHA and ARA. Journal of pediatric gastroenterology and nutrition 2008;47 Suppl 2():S60-1
http://dx.doi.org/10.1097/01.mpg.0000338817.90180.a0 https://pubmed.ncbi.nlm.nih.gov/18931605[134] Venter C, Pereira B, Voigt K, Grundy J, Clayton CB, Higgins B, Arshad SH, Dean T. Prevalence and cumulative incidence of food hypersensitivity in the first 3 years of life. Allergy 2008;63(3):354-9
https://pubmed.ncbi.nlm.nih.gov/18053008[135] von Berg A, Filipiak-Pittroff B, Krämer U, Link E, Bollrath C, Brockow I, Koletzko S, Grübl A, Heinrich J, Wichmann H-E, Bauer C-P, Reinhardt D, Berdel D, . Preventive effect of hydrolyzed infant formulas persists until age 6 years: long-term results from the German Infant Nutritional Intervention Study (GINI). The Journal of allergy and clinical immunology 2008;121(6):1442-7
http://dx.doi.org/10.1016/j.jaci.2008.04.021 https://pubmed.ncbi.nlm.nih.gov/18539195[136] von Berg A, Koletzko S, Filipiak-Pittroff B, Laubereau B, Grübl A, Wichmann H-E, Bauer C-P, Reinhardt D, Berdel D, . Certain hydrolyzed formulas reduce the incidence of atopic dermatitis but not that of asthma: three-year results of the German Infant Nutritional Intervention Study. The Journal of allergy and clinical immunology 2007;119(3):718-25
https://pubmed.ncbi.nlm.nih.gov/17240440[137] West CE, Hammarström M-L, Hernell O. Probiotics during weaning reduce the incidence of eczema. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2009;20(5):430-7
http://dx.doi.org/10.1111/j.1399-3038.2009.00745.x https://pubmed.ncbi.nlm.nih.gov/19298231[138] Willemsen MG, van Valburg RWC, Dirven-Meijer PC, Oranje AP, van der Wouden JC, Moed H. Determining the severity of atopic dermatitis in children presenting in general practice: an easy and fast method. Dermatology research and practice 2009;2009():357046
http://dx.doi.org/10.1155/2009/357046 https://pubmed.ncbi.nlm.nih.gov/20585477[139] Wilt TJ, Shaukat A, Shamliyan T, Taylor BC, MacDonald R, Tacklind J, Rutks I, Schwarzenberg SJ, Kane RL, Levitt M. Lactose intolerance and health. Evidence report/technology assessment 2010
https://pubmed.ncbi.nlm.nih.gov/20629478[140] Wolraich ML, Wilson DB, White JW. The effect of sugar on behavior or cognition in children. A meta-analysis. JAMA 1995;274(20):1617-21
https://pubmed.ncbi.nlm.nih.gov/7474248[141] Wood RA. The natural history of food allergy. Pediatrics 2003;111(6 Pt 3):1631-7
https://pubmed.ncbi.nlm.nih.gov/12777603[142] Zutavern A, Brockow I, Schaaf B, Bolte G, von Berg A, Diez U, Borte M, Herbarth O, Wichmann H-E, Heinrich J, . Timing of solid food introduction in relation to atopic dermatitis and atopic sensitization: results from a prospective birth cohort study. Pediatrics 2006;117(2):401-11
https://pubmed.ncbi.nlm.nih.gov/16452359[143] Zutavern A, Brockow I, Schaaf B, von Berg A, Diez U, Borte M, Kraemer U, Herbarth O, Behrendt H, Wichmann H-E, Heinrich J, . Timing of solid food introduction in relation to eczema, asthma, allergic rhinitis, and food and inhalant sensitization at the age of 6 years: results from the prospective birth cohort study LISA. Pediatrics 2008;121(1):e44-52
http://dx.doi.org/10.1542/peds.2006-3553 https://pubmed.ncbi.nlm.nih.gov/18166543[144] Zutavern A, von Mutius E, Harris J, Mills P, Moffatt S, White C, Cullinan P. The introduction of solids in relation to asthma and eczema. Archives of disease in childhood 2004;89(4):303-8
https://pubmed.ncbi.nlm.nih.gov/15033835[145] Anonymous (2007). Artificial colors and hyperactivity
http://www.food.gov.uk.[146] Anonymous (2008a). Diagnostiek van Koemelkallergie in Nederland: Anders.
[147] Anonymous (2008b). Verordening EG 1333/2008. In (Anonymous).
http://Eur-lex.europa.eu.[148] Anonymous (2011). Multidisciplinaire richtlijn: Excessief huilen bij zuigelingen (in ontwikkeling). In (Anonymous). TNO, Leiden.
[149] CBO (2006). Richtlijn Constitutioneel eczeem.
[150] CBO (2008). Richtlijn Coeliakie en Dermatitis Herpetiformis.
[151] Chafen JJS, Newberry SJ, Riedl M, Bravata DM, Maglione MA, Booth M, Sundaram V, Paige NM, Towfigh A, Hulley BJ, Shekelle PG. Prevalence, Natural History, Diagnosis, and Treatment of Food Allergy: A Systematic Review of the Evidence (null) 2010
https://www.rand.org/pubs/working_papers/WR757-1.html[152] Büchner FL, Ezendam J, Tijhuis MJ, Mennes W, van Loveren H, van den Berg SW. Voeding en ADHD Diet and ADHD 2010
[153] Commissie ‘Standaard’. Landelijke standaard voor de diagnose en behandeling van voedselovergevoeligheid bij zuigelingen op het consultatiebureau. LIVO: Den Haag. 1994
[154] Gezondheidsraad. Voedselallergie 2007
[155] Kamphuis M.. JGZ-richtlijn Huidafwijkingen. 2012
http://www.ncj.nl/bibliotheek/%20richtlijnen/[156] Kneepkens CMF, van Drongelen KI, Aarsen CJE. Landelijke standaard voedselallergie bij zuigelingen; standaard voor de diagnose, behandeling en preventie van voedselallergie bij zuigelingen op het consultatiebureau. In (Anonymous). 2005
[157] Kramer MS, Kakuma R. Maternal dietary antigen avoidance during pregnancy or lactation, or both, for preventing or treating atopic disease in the child. The Cochrane database of systematic reviews 2012;2012(9):CD000133
http://dx.doi.org/10.1002/14651858.CD000133.pub3 https://pubmed.ncbi.nlm.nih.gov/22972039[158] Lucassen P. Colic in infants. BMJ clinical evidence 2010;2010():
https://pubmed.ncbi.nlm.nih.gov/21729336[159] Lucassen P, Albeda F, van Reisen M, Silvius A, Wensing C, Luning-Koster M. M47NHG-Standaard Voedselovergevoeligheid Huisarts En Wetenschap 2010;53():537
http://dx.doi.org/10.1007/BF03089284[160] Meijer Y., Brand P.L.P., Duijvestijn Y.C.M., Vlieg-Boerstra B.J.. Diagnostiek naar voedselallergie in de tweede lijn: Consensusstandpunt sectie kinderallergologie. Tijdschrift voor Kindergeneeskunde, 78(6), 237-243. 2010
https://doi.org/10.1007/s12456-010-0057-5[161] Mofidi S., Bock S.A.. The Food Allergy & Anaphylaxis Network. A Health professional’s guide to food challenges. In (Anonymous). 2005
[162] National Institute for Health and Clinical Excellence (NICE). Coeliac disease. Recognition and assessment of coeliac disease. Clinical Guideline. 2009
[163] National Institute for Health and Clinical Excellence. (2011). NICE clinical guideline 116 – Food allergy in children and young people National Institute for Health and Clinical Excellence (2011). Diagnosis and assessment of food allergy in children and young people in primary care and community settings. In (Anonymous), London. 2011
[164] Olives J-P. [When should we introduce gluten into the feeding of the new-born babies?]. Archives de pediatrie : organe officiel de la Societe francaise de pediatrie 2010;17 Suppl 5():S199-203
http://dx.doi.org/10.1016/S0929-693X(10)70927-1 https://pubmed.ncbi.nlm.nih.gov/21300263[165] RIVM. Rijksvaccinatieprogramma. 2012
[166] Sprikkelman A., Vlieg-Boerstra B., Kneepkens C.. Diagnostiek van Koemelkallergie bij kinderen in Nederland. Utrecht, Nederlandse Vereniging voor Kindergeneeskunde. 2012
http://www.nvk.nl[167] Stichting Nationaal Programma Grieppreventie (2012). In (Anonymous).
[168] van den Berg S.W., Büchner F.L., Boer J.M.A., Ezendam J., Mennes W., van Loveren H., Verhagen H.. Voeding en ADHD: beoordeling van de INCA-studie. Bilthoven. 2011
[169] Vlieg-Boerstra BJ, Meijer Y.. Dubbelblinde voedselprovocaties Tijdschrift voor Kindergeneeskunde 2008;76(2):66
http://dx.doi.org/10.1007/BF03078182 https://doi.org/10.1007/BF030781821 Inleiding
Voedselovergevoeligheid is een ongewenste reproduceerbare reactie ten gevolge van allergie (bv. koemelkallergie), afwijkende (auto-)immuunrespons (coeliakie) of intolerantie (bv. lactose-intolerantie) voor een voedingsbestanddeel. Er bestaat geen (medicamenteuze) therapie voor voedselallergie, zodat preventie (waar mogelijk) van belang is.
Deze richtlijn geeft adviezen over de preventie en het signaleren van voorkomende oorzaken van voedselovergevoeligheid in de jeugdgezondheidszorg. De diagnostiek van koemelkallergie is afgestemd met de aanpalende disciplines huisarts en kinderarts en is overgenomen uit de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’ [166].
Bij velen leeft de gedachte dat voedseladditieven het gedrag van een kind in negatieve zin beïnvloeden. De richtlijn gaat in op de vraag of hier wetenschappelijk bewijs voor is.
1.1 Voorwoord
Voor u ligt de JGZ-richtlijn Voedselovergevoeligheid. De richtlijn ‘Diagnostiek van Koemelk-allergie bij Kinderen in Nederland’ van de Nederlandse Vereniging voor Kindergeneeskunde maakt hier onderdeel van uit [166]. De richtlijn Voedselovergevoeligheid vervangt de Landelijke Standaard voedselallergie bij zuigelingen [156]. Als uitgangspunt voor de richtlijn geldt het rapport Voedselallergie van de Gezondheidsraad [154].
Zowel de verbeterde diagnostiek van koemelkallergie als de samenwerking en afstemming tussen de jeugdgezondheidszorg, huisartsen en kinderartsen zijn belangrijke verbeteringen.
Toen ik me specialiseerde tot kinderarts (1976-1980) was voedselallergie controversieel. Er werd niet of nauwelijks over gesproken. Ook met ouders werd niet gecommuniceerd.
Er ligt nu een geweldig stuk met evidence-based informatie over voedselovergevoeligheid. Er is veel meer bekend. Diagnostiek en behandeling zijn sterk verbeterd. En is er nu veel meer mogelijk dan vroeger. Dat staat in deze richtlijn. Velen hebben aan de totstandkoming hiervan bijgedragen. De betrokkenheid en deskundigheid van de diverse partijen waren hoog, de samenwerking goed en de prestatie doelgericht. Een grote stap voorwaarts.
Vooral voor ouders is deze richtlijn van groot belang. Met de ouders wordt gericht gezocht naar een oplossing. Dat zal een geruststelling zijn.
Nieuw is dat de diagnostiek door de JGZ zal worden uitgevoerd, dicht bij huis in de vertrouwde omgeving.
Rest mij allen die aan deze richtlijn hebben gewerkt hartelijk te danken. Het is TOP. We gaan ermee aan de slag. Ik ben ervan overtuigd dat wij hiermee een belangrijke bijdrage leveren aan het behoud van de gezondheid van vele kinderen.
Remy HiraSing
VUmc/EMGO+,Amsterdam
1.2 Doelstelling
Het doel van de richtlijn Voedselovergevoeligheid is het voorkomen en vroeg signaleren van voedselovergevoeligheid, en het begeleiden en zo nodig verwijzen van kinderen met voedselovergevoeligheid naar huisarts of specialist. De richtlijn is geschreven voor jeugdartsen, jeugdverpleegkundigen, verpleegkundig specialisten en doktersassistenten werkzaam in de JGZ. De aanpak van voedselovergevoeligheid in de JGZ moet goed aansluiten bij het beleid van huisartsen, kinderartsen en diëtisten.
Met deze richtlijn kan de JGZ-professional volgens de huidige stand van de wetenschap:
- adviezen voor preventie van voedselovergevoeligheid geven;
- kinderen met voedselovergevoeligheid tijdig signaleren;
- kinderen met koemelkallergie diagnosticeren;
- kinderen met koemelkallergie begeleiden of zo nodig verwijzen.
1.3 Leeswijzer
De JGZ-richtlijn Voedselovergevoeligheid bestaat uit 3 delen.
Voor u ligt de volledige richtlijn, waarin u de wetenschappelijke onderbouwing van de aanbevelingen kunt vinden.
Voor de praktijk van de JGZ zijn er een samenvatting van de richtlijn en een kaart met de belangrijkste elementen. Hierin vindt u praktische handvatten voor preventie, signalering, verwijzing en interventie bij kinderen met voedselovergevoeligheid.
In de bijlagen bij de samenvatting staat informatie voor ouders en protocollen voor voedselprovocatietesten voor de praktijk.
2 Definitie en achtergrondinformatie
Voedselovergevoeligheid is een ongewenste reproduceerbare reactie ten gevolge van allergie (bv. koemelkallergie), afwijkende (auto-)immuunrespons (coeliakie) of intolerantie (bv. lactose-intolerantie) voor een voedingsbestanddeel. Er bestaat geen (medicamenteuze) therapie voor voedselallergie, zodat preventie (waar mogelijk) van belang is.
2.1 Prevalentie voedselallergie
De prevalentie van voedselallergie bij kinderen tot 3 jaar is 4-8% [3]; [15]. Prevalentiecijfers zijn echter afhankelijk van de onderzoeksmethode. Zelfrapportage van symptomen geeft een veel hogere prevalentie vergeleken met onderzoek waarbij ook sensibilisatie (serum IgE) en/of dubbelblind placebogecontroleerde voedselprovocatie wordt betrokken [22]. Er lijkt geen toename van de prevalentie van voedselallergie in de tijd te zijn, maar meer onderzoek is nodig om hier duidelijkheid over te krijgen [151].
Kinderen met voedselallergie hebben over het algemeen 2-4 keer meer kans op andere atopische aandoeningen zoals astma (4,0 keer) en atopische dermatitis (2,4 keer) vergeleken met kinderen zonder voedselallergie [22].
2.2 Koemelkallergie
Koemelkallergie bij zuigelingen is de meest frequente vorm van voedselallergie: de prevalentie in Nederland is 2-3% [76]. Koemelkallergie gaat vaak gepaard met maag-/darmklachten (braken, diarree, kolieken), huidverschijnselen (constitutioneel eczeem, urticaria) en een enkele keer met algemene verschijnselen zoals ontroostbaar huilen [42]. Over het algemeen zijn de problemen van voorbijgaande aard; op de leeftijd van 3 jaar heeft 90% van de kinderen geen klachten meer.
Van deze kinderen ontwikkelt 25-58% andere voedselallergieën, zoals voor kippenei, pinda’s, noten, appel, soja, sesamzaad, vis, schaal- en schelpdieren [37]; [141]. De verschijnselen kunnen variëren van urticarieel exantheem tot benauwdheid en anafylactische shock.
Bij twee derde van de kinderen met een kippeneiallergie zijn de klachten verdwenen op de leeftijd van 16 jaar.
Pinda-allergie persisteert bij 80-90% van de kinderen levenslang met soms ernstige, zelfs dodelijke allergische reacties [25]; [79]. Ongeveer 5% van de kinderen met een pinda-allergie krijgt na inname van pinda’s een anafylactische reactie (Rance et al., 1999).
Daarnaast is bij de helft van de kinderen koemelkallergie een onderdeel van een atopische constitutie met constitutioneel eczeem, hooikoorts en/of astma [3].
2.3 Lactose-intolerantie
Lactose-intolerantie wordt veroorzaakt door een tekort aan lactase, het enzym dat lactose afbreekt. Het eten/drinken van lactosebevattend voedsel (bv. melk, vla, yoghurt) bij lactose-intolerantie uit zich in buikpijn, flatulentie en diarree. Hypolactasie (vroeger primaire lactasedeficiëntie genoemd) komt bij vele etnische groepen voor, maar geeft over het algemeen weinig klachten [56].
2.3.1 Achtergrondinformatie
Lactose (melksuiker) is het belangrijkste koolhydraat in moedermelk en in de melk van dieren, in de eerste plaats koemelk. Het lactosegehalte in moedermelk is 70 g/l, in koemelk 50 g/l. Lactose komt niet of nauwelijks voor in andere natuurlijke producten en het lactoseaanbod is voor alle zoogdieren dus beperkt tot de zoogperiode. Lactose vormt zo een essentieel bestanddeel van de voeding van jonge zuigelingen.
Voor de vertering van lactose is een borstelzoomenzym in de darmen nodig, lactase. De splitsingsproducten glucose en galactose worden door actief transport geabsorbeerd. Na de zoogtijd daalt het lactasegehalte in de borstelzoom bij alle zoogdieren sterk. Deze ‘down-regulatie’ is genetisch bepaald. Bij de mens leidt dit tot hypolactasie of lactase non-persistence, vroeger ook wel primaire lactasedeficiëntie genoemd.
De afname van het lactasegehalte begint bij verschillende rassen op verschillende tijden en verloopt met verschillende snelheden. Bij Aziatische rassen is de basale activiteit eerder (5-6 jaar) bereikt dan bij blanken met hypolactasie (20 jaar). Bij een deel van de mensheid treedt deze natuurlijke daling van het lactasegehalte niet op: lactasepersistentie. Dit wordt veroorzaakt door een mutatie (SNP) in een niet-coderend gebied in intron 13 van MCM6, C/T-13910, gelegen 13910 baseparen stroomopwaarts van het lactasegen LCT op chromosoom 2q21-22. Het normale genotype, C/C-13910, gepaard gaande met hypolactasie, komt voor bij 70% van de wereldbevolking; blanken zijn over het algemeen lactasepersistent ([68]).
Lactosemalabsorptie
Bij optimale lactaseactiviteit is de darm in staat om alle via de voeding aangevoerde lactose nagenoeg volledig te verteren en absorberen. Als het lactoseaanbod met de voeding de verwerkingscapaciteit (lactaseactiviteit) van de dunne darm overtreft, komt een deel van de lactose terecht in het colon, waar dit, net als alle andere koolhydraten, inclusief zetmeel en voedingsvezel, kan worden afgebroken (gefermenteerd) door de residente bacteriën (microbiota). Bij deze vergisting komt onder meer waterstof vrij, dat voor een groot deel via de longen wordt uitgeademd. Dit proces is gemakkelijk te meten; bij lactosemalabsorptie is de lactose-waterstofademtest afwijkend. Aangezien deze vergisting in principe een fysiologisch proces is, gaat lactosemalabsorptie meestal niet gepaard met klachten. Klachten ontstaan pas als de fermentatieve capaciteit van de microbiota (de colonic salvage) wordt overschreden.
Lactose-intolerantie
Lactose-intolerantie kan worden gedefinieerd als lactosemalabsorptie die gepaard gaat met klachten. De klachten van koolhydraatmalabsorptie over het algemeen berusten op de aanwezigheid van een overmaat aan onvolledig gefermenteerde koolhydraten in het colon: in minder ernstige gevallen opgeblazen gevoel, buikpijn en flatulentie, in ernstiger gevallen osmotische diarree. De relatie tussen lactosemalabsorptie en lactose-intolerantie varieert aanzienlijk van individu tot individu, maar lactose-intolerantie ontstaat over het algemeen pas bij de consumptie van 12-15 g lactose (240-300 ml melk) ([139]).
Secundaire lactosemalabsorptie
Alle acute en chronische vormen van enteropathie met aantasting van de proximale dunne darm leiden tot malabsorptie van nutriënten. Van de borstelzoomenzymen is vooral lactase erg gevoelig voor de integriteit van de mucosa. Aantasting van de mucosa leidt snel tot daling van de lactaseactiviteit en tot lactosemalabsorptie. Bij acute pathologie, zoals acute gastro-enteritis, herstelt de absorptiecapaciteit zich even snel als het darmslijmvlies. Bij chronische pathologie, zoals coeliakie, treedt meestel compensatie op door hypertrofie van vlokken en toegenomen lactaseactiviteit meer distaal in de darm. Secundaire lactosemalabsorptie is dan ook zelden of nooit een klinisch relevant probleem. Klachten worden voornamelijk veroorzaakt door de onderliggende ziekte.
2.4 Glutenovergevoeligheid (Coeliakie)
Overgevoeligheid voor gluten (coeliakie) is een multisysteem inflammatoire (auto-)immuunziekte die kan optreden bij erfelijk gepredisponeerde mensen na ingestie van gluten. Coeliakie komt in Nederland bij 1 op de 200 kinderen voor [30]. De klinische presentatie is erg verschillend; het topje van de ijsberg wordt gevormd door kinderen met klinisch gediagnosticeerde coeliakie met symptomen van chronische diarree en tekenen van malabsorptie en/of kleine lengte [150]. Sommige kinderen (en volwassenen) hebben echter weinig of geen klachten. Op de lange termijn is er vooral bij niet-gediagnosticeerde en niet-behandelde patiënten een verhoogde kans op osteoporose, andere auto-immuunziekten (diabetes mellitus type 1, hypo-/hyperthyreoïdie), leverfunctiestoornissen, fertiliteitsstoornissen en kanker [21]; [47]; [52].
2.4.1 Achtergrondinformatie
Coeliakie is een immuungemedieerde systemische aandoening die wordt uitgelokt door gluten en verwante prolaminen bij personen met een daarvoor gevoelige genetische aanleg en wordt gekenmerkt door een variabele combinatie van glutengeïnduceerde symptomen, specifieke antistoffen, een specifiek haplotype (HLA-DQ2 of -DQ8) en enteropathie ([60]). Deze nieuwe definitie vervangt voorgaande definities, waarbij enteropathie meer centraal stond.
Het HLA-haplotype is verreweg de belangrijkste, maar niet de enige genetische risicofactor; er zijn inmiddels tientallen genen bekend die de kans op coeliakie beïnvloeden. 95% van de coeliakiepatiënten is drager van HLA-DQ2.5; bij de resterende 5% is DQ8 of DQ2.2 aanwezig. Dit betekent dat 30-40% van de Nederlandse bevolking coeliakie kan ontwikkelen. In werkelijkheid komt coeliakie voor bij 1 op de 200 personen en ligt de huidige incidentie van gediagnosticeerde coeliakie bij kinderen tussen de 1 en 2 per 1000 ([30]; [124]). Klinisch uit de aandoening zich zeer variabel, van (vrijwel) symptoomloos tot ernstige dystrofie.
Voor het optreden van coeliakie is de ingestie van gluten als initiërende factor essentieel, maar de aandoening kan ontstaan op elke leeftijd na de introductie van gluten in het dieet. Bepaalde glutenpeptiden worden herkend door HLA-DQ2 en of HLA-DQ8 op antigeenpresenterende cellen, waarna T-cellen worden geactiveerd. Deaminering van de glutamineresiduen in de glutenpeptiden tot glutaminezuur door het enzym transglutaminase type 2 versterkt de antigene eigenschappen ervan. Hierdoor komt de afweerreactie pas goed op gang. Lymfocyten concentreren zich in het darmepitheel en ontketenen daar een ontstekingsproces dat leidt tot de enteropathie, zich uitend in cryptehyperplasie en vervolgens vlokatrofie. De afweerreactie gaat gepaard met de vorming van antilichamen tegen gliadinepeptiden, endomysium en transglutaminase type 2.
2.5 Voedseladditieven
Additieven zoals kleurstoffen en conserveermiddelen worden aan voedingsmiddelen toegevoegd om de eigenschappen van een product te verbeteren of te veranderen. Sommige ouders vermoeden dat hun kind druk gedrag vertoont na het eten van kunstmatige kleurstoffen.
2.5.1 Achtergrondinformatie
Additieven zoals kleurstoffen en conserveermiddelen worden aan voedingsmiddelen toegevoegd om de eigenschappen van een product te verbeteren of te veranderen. Er zijn vele verschillende synthetische kleurstoffen, bv. tartrazine (citroengeel, E102), oranje-geel (E110), karmozijnrood (E122) en briljantblauw (E133). Deze kleurstoffen worden met name gebruikt in snoep, koekjes en toetjes, maar komen in vele gekleurde voedingsmiddelen voor. Natriumbenzoaat is een veelgebruikt conserveermiddel, het werkt goed bij een lage pH zoals in jam, frisdranken en vruchtensappen, maar wordt ook toegevoegd aan brood, broodbeleg en vele kant-en-klare producten.
In de jaren 70 propageerde Feingold een eliminatiedieet voor kinderen met een ‘attention deficit hyperactivity disorder’ (ADHD) ([40]). Het dieet was gebaseerd op de hypothese dat kinderen met hyperactiviteit een voedselintolerantie hebben en dat het elimineren van bepaalde additieven zoals kunstmatige kleur- en smaakstoffen en natuurlijk voorkomende salicylaten gedragsproblemen kan verminderen en het leren kan verbeteren. Het onderzoek van Feingold kreeg veel kritiek, met name vanwege het ontbreken van een controlegroep. Sindsdien zijn meerdere studies verschenen, waarvan vele niet gerandomiseerd, placebogecontroleerd en/of dubbelblind zijn. Over het algemeen betreffen het studies met kleine aantallen kinderen.
2.6 Risicofactoren
Uit de reviews van lage tot matige kwaliteit kwamen de volgende risicofactoren naar voren voor het ontwikkelen van voedselallergie:
- atopische ziekten bij ouders of broertjes/ zusjes (lage kwaliteit)
- vroeg optreden van constitutioneel eczeem en ernstig constitutioneel eczeem (matige kwaliteit)
- vroege blootstelling aan voedselallergenen via de borstvoeding en via het dieet van de moeder (tegenstrijdig bewijs van lage kwaliteit),
- keizersnede (variabel bewijs van lage tot matige kwaliteit),
- oken door de moeder tijdens de zwangerschap (lage kwaliteit)
- symptomen van huid, maag en darmen en anafylaxie (lage kwaliteit).
Zie verder Symptomen Koemelkallergie.
2.7 Afkortingen
| AA | kunstvoeding op basis van vrije aminozuren |
| AJN | Artsen Jeugdgezondheidszorg Nederland |
| DBPGVP | dubbelblinde placebogecontroleerde voedselprovocatie |
| eHF | intensief gehydrolyseerde kunstvoeding |
| eHF-C | intensief gehydrolyseerde kunstvoeding op caseïnebasis |
| eHF-W | intensief gehydrolyseerde kunstvoeding op wei-eiwitbasis |
| HA | huisarts |
| JGZ | jeugdgezondheidszorg |
| NCJ | Nederlands Centrum Jeugdgezondheid |
| NHG | Nederlands Huisartsen Genootschap |
| NVD | Nederlandse Vereniging van Diëtisten |
| NVK | Nederlandse Vereniging voor Kindergeneeskunde |
| OVP | open voedselprovocatie |
| RCT | randomised controlled trial |
| SF | kunstvoeding op basis van soja |
| SR | systematische review |
| V&VN | Verpleegkundigen & Verzorgenden Nederland |
3 Preventie, Signaleren en verwijzen.
3.1 Koemelk-allergie
Uit de knelpuntenanalyse komt naar voren dat er enerzijds (te) snel wordt gedacht aan koemelkallergie en er onduidelijkheid is over de vaak aspecifieke symptomen. Anderzijds komt het voor dat in de praktijk kinderen met een verhoogd risico op ernstige reacties op koemelk niet tijdig worden herkend. Hierdoor bestaat enerzijds de kans op overdiagnostiek en anderzijds wordt bij een kleine groep kinderen de diagnose koemelkallergie laat gesteld.
Aanbevelingen
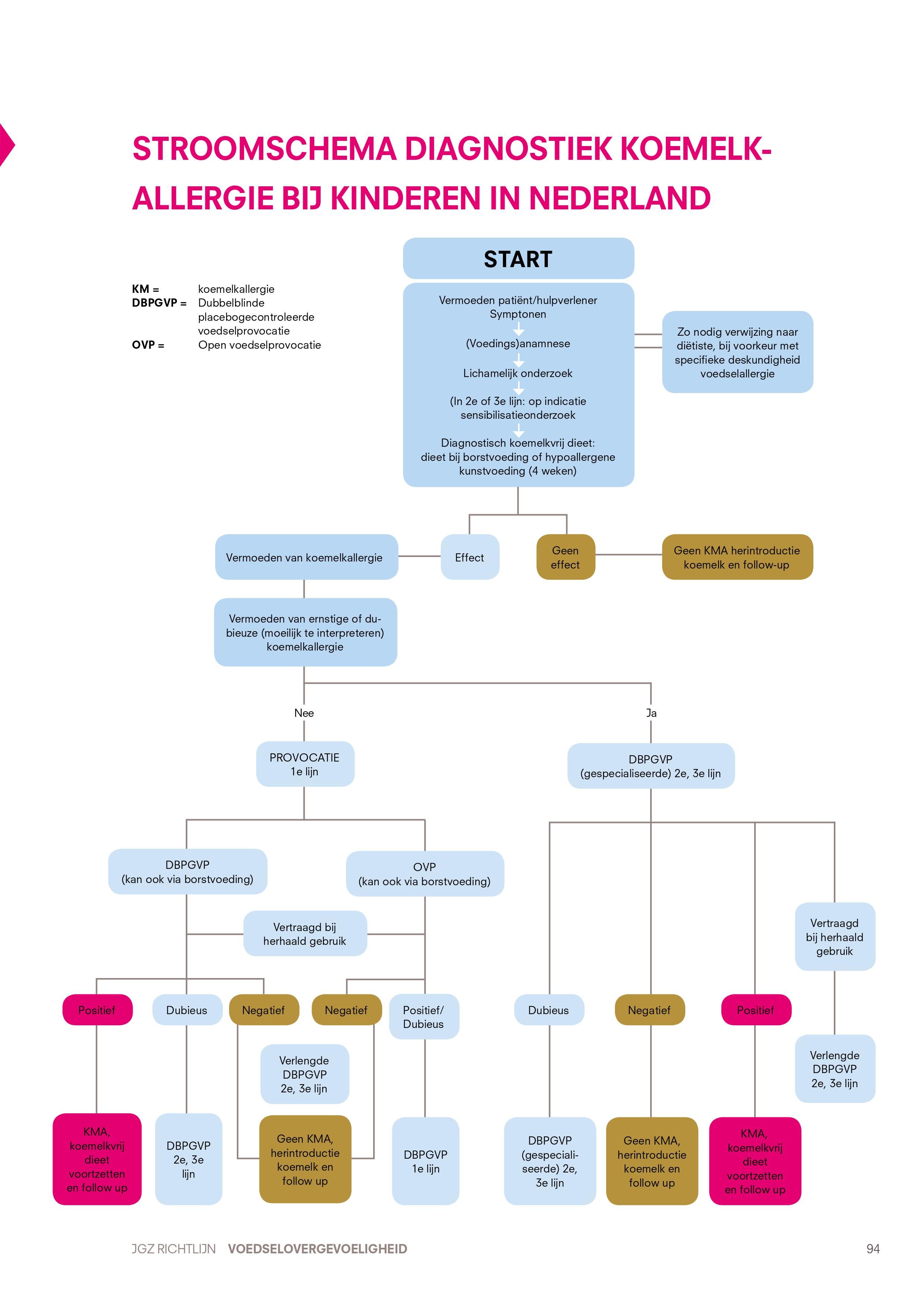
3.1.1 Stroomschema diagnostiek koemelkallergie bij kinderen in Nederland
3.1.2 Symptomen Koemelkallergie
Kinderen met koemelkallergie kunnen zich presenteren met een breed scala aan klachten, vaak van meerdere orgaansystemen. Geen enkel symptoom is specifiek voor de diagnose koemelkallergie. Overweeg de mogelijkheid van koemelkallergie bij patiënten die een of meer van de symptomen hebben uit tabel 3.3.1.
In deze tabel zijn de meest voorkomende symptomen van koemelkallergie weergegeven. Meestal zijn het maag-darmkanaal, de huid of de luchtwegen betrokken. Opzichzelfstaande luchtwegklachten hebben zelden een relatie met koemelkallergie. Omdat geen enkel symptoom specifiek is voor koemelkallergie, moet differentiaaldiagnostisch worden gedacht aan andere oorzaken voor de klachten, zoals voedingsfouten, virale infecties en dergelijke.
Ondanks dat de kwaliteit van het bewijs van (voedings)anamnese en afwijkingen gevonden bij lichamelijk onderzoek laag is, heeft de werkgroep besloten om de symptomen uitgebreid weer te geven en differentiaaldiagnostisch ook andere oorzaken die de klachten kunnen veroorzaken te benoemen.
Tevens is op basis van de ernst van de klinische symptomen een tweedeling gemaakt in patiënten die gediagnosticeerd en begeleid kunnen worden in de JGZ en kinderen die voor diagnostiek en behandeling verwezen moeten worden naar de huisarts/kinderarts.
Tabel 3.3.1 Symptomen die kunnen wijzen op koemelkallergie (National Institute for Health and Clinical Excellence, 2011)
|
Directe symptomen (ontstaan binnen minuten/uren) |
Late symptomen (ontstaan na enkele uren) |
Differentiaaldiagnose
|
| Huid | ||
| jeuk | jeuk | |
| erytheem | erytheem | infectie |
| urticaria | infectie (meestal viraal), idiopathische urticaria, aspecifieke oorzaken zoals koude, warmte, zon of druk | |
| angio-oedeem (lippen, gelaat, rondom ogen) | toename van constitutioneel eczeem | (vluchtig) exantheem, prikkelende middelen, temperatuurwisselingen, bacteriële infectie, vluchtige peri-orale roodheid tijdens of na het eten |
| Gastro-intestinaal | ||
| jeuk in de mond | ||
| angio-oedeem (lippen, tong en gehemelte) | ||
| krampende buikpijn | buikpijn | infectie, gastro-oesofagale reflux, obstipatie, invaginatie, verkeerde drinktechniek, ouder-kindinteractie |
| misselijkheid, spugen | misselijkheid, spugen, gastro-oesofagale reflux | voedingsfouten (te veel of te snel voeden, verkeerde samenstelling van de voeding), aversie, regurgitatie, gastro-oesofagale reflux, infectie (bv. urineweginfectie), pylorushypertrofie |
| diarree | frequente stoelgang van afwijkende consistentie | gastro-enteritis of andere infecties, voedingsfouten (zie braken, misselijkheid), tijdelijke lactose-intolerantie, coeliakie, cystische fibrose |
| bloed en/of slijm bij de ontlasting | gastro-enteritis, invaginatie, divertikel | |
| obstipatie | functionele obstipatie, ziekte van Hirschsprung | |
| Luchtwegen (vaak in combinatie met huid- en/of gastro-intestinale symptomen) | ||
| bovensteluchtwegklachten: jeuk aan de neus, niezen, loopneus, verstopte neus (met of zonder conjunctivitis) | virale infectie | |
| inspiratoire stridor (bij larynx-oedeem) | virale of bacteriële infectie, aspiratie corpus alienum | |
| lagereluchtwegklachten: hoesten, dyspnoe | virale of bacteriële infectie, aspiratie corpus alienum | |
| Cardio-vasculair | ||
| symptomen van anafylaxie: tachy-/bradycardie, hypotensie, shock, verminderd bewustzijn | bacteriële of virale infectie (sepsis, meningitis), andere allergie (bv. geneesmiddel of insecten), vergiftiging | |
| Overige | ||
| voedselweigering | voedselweigering | infectie, overvoeding, psychosociale factoren |
| bleekheid en moeheid | ||
| afbuigende groei in combinatie met gastro-intestinale symptomen (met of zonder ernstig constitutioneel eczeem | voedingsfouten, malabsorptie, coeliakie, giardiasis, cystische fibrose etc. | |
| huilen, onrust | verkeerde drinktechniek, verzorgingsfouten (bv. te weinig voeding), te veel prikkels, ouder-kindinteractie, pijn (bv. otitis media) | |
De belangrijkste symptomen die kunnen wijzen op koemelkallergie:
Directe symptomen van de huid (rode uitslag, jeuk, zwelling, urticaria), maag en darmen (spugen, diarree) en luchtwegen (benauwdheid, piepen, rinitis) in relatie tot de inname van koemelk en zonder andere verklaring.
Vertraagde symptomen bestaande uit toename van matig tot ernstig constitutioneel eczeem (TIS-score > 3), bloederige ontlasting, voedselweigering en afbuigende groei.
Er is geen sterk vermoeden van koemelkallergie bij uitsluitend:
- excessief huilen en prikkelbaar gedrag;
- obstipatie;
- klachten die zouden kunnen passen bij gastro-oesofagale reflux. ([148]; [62]; Lucassen, 2010; [125])
Er is geen vermoeden van koemelkallergie bij mild constitutioneel eczeem dat goed reageert op lokale corticosteroïden.
3.1.3 Effecten van de interventies
Dieet van moeder gedurende de zwangerschap of lactatie
In een systematische review ([157]) van goede kwaliteit waarin 4 studies werden geïncludeerd (n = 334) werd geen beschermend effect gevonden na 18 maanden voor het dieet (waarin antigenen werden vermeden) van de moeder. De geïncludeerde studies waren van beperkte methodologische kwaliteit. Twee studies ([54]; [120]) rapporteerden over een niet-gerandomiseerde trial (n = 115) van lage methodologische kwaliteit. Zij vonden een significant gereduceerde incidentie van atopische dermatitis na 18 maanden en 4 jaar bij kinderen met een dubbele erfelijke belasting wiens moeder een restrictief dieet (vrij van koemelk, kippeneieren en visproducten gedurende 3 maanden na de geboorte) volgde tijdens lactatie.
Exclusieve borstvoeding
Drie analyses ([41]; [81]; [116]) van hetzelfde cohort (n = 4753) lieten tegenstrijdige effecten zien van exclusieve borstvoeding op de preventie van atopische ziekten (twee van deze studies rapporteerden verminderde atopische dermatitis bij kinderen met een positieve familieanamnese van atopie die alleen borstvoeding kregen vergeleken met kinderen bij wie dit niet het geval was). De methodologische kwaliteit van deze studies was laag (slechts 1 niet-gerandomiseerde studie)
Borstvoeding en het uitstellen van de introductie van de eerste bijvoeding
Twee studies ([53]; n = 696) en [71]; n = 113)) bij kinderen met atopische ouders vonden een beperkte associatie tussen het uitstellen van de eerste bijvoeding (tot 6 maanden) en de incidentie van atopische symptomen (door de ouders gerapporteerde verminderde voedseltolerantie) [53] en (niet-significante) hogere incidentie van atopie in de controlegroep [71]. De resultaten van de studies dienen met terughoudendheid geïnterpreteerd te worden gegeven de multimodale opzet en de lage methodologische kwaliteit.
Speciale diëten voor zuigelingen en jonge kinderen
Kunstvoeding op basis van sojamelk versus kunstvoeding op basis van koemelk
De effecten van sojamelk ter preventie van atopie werden vergeleken met de effecten van kunstvoeding op basis van koemelk in een SR [97] en een RCT [10] bij kinderen met een hoog risico op atopie. Er was weinig verschil tussen kunstvoeding op basis van sojamelk en kunstvoeding op basis van koemelk ter preventie van allergieën bij de kinderen met een hoog risico.
Blootstelling aan koemelk
In drie RCT’s ([33]; [32]; [82]) werd vroege blootstelling aan koemelk geëvalueerd in twee verschillende borstgevoede populaties (zuigelingen met en zonder laag geboortegewicht) waarbij geen verschillen werden gevonden in de prevalentie van atopie. De methodologische kwaliteit van de studies was laag.
Gehydrolyseerde kunstvoeding versus niet-gehydrolyseerde kunstvoeding op basis van koemelk of borstvoeding
Twee SR’s [55]; [96] en drie RCT’s ([7]; [95]; [126]; [136]; [135]) evalueerden de effecten van gehydrolyseerde kunstvoeding op het ontwikkelen van voedselallergieën bij kinderen met een hoog risico. Gehydrolyseerde kunstvoeding (intensief en partieel) zou in vergelijking met niet-gehydrolyseerde zuigelingenvoeding op basis van koemelk een preventief effect hebben op koemelkallergie bij kinderen met een hoog risico. Er was echter sprake van een onduidelijke definitie van intensief en partieel en van de groep hoogrisicokinderen. De gewenste en ongewenste effecten van vroege expositie aan koemelk blijven onduidelijk. De studies van Von Berg ([136]; [135]) zijn omstreden vanwege methodologische tekortkomingen. Alleen in de studie van Odelram et al. ([95]) werd een vergelijking gemaakt tussen gehydrolyseerde voeding en borstvoeding, maar er werden geen significante verschillen gevonden.
In de review van Chafen [151] werden alleen de preventieve effecten beschreven van probiotica. Voor de beschrijving van de effecten van prebiotica wordt gebruik gemaakt van de review van Van der Aa [131]. Onder prebiotica wordt verstaan: niet-verteerbare oligosachariden die de groei van gezondheidbevorderende bacteriën (bv. bifidus-/lactobacillus) in de darm kunnen bevorderen. Onder probiotica wordt verstaan: niet-pathogene bacteriën die van nature aanwezig zijn in de darm en die de gezondheid positief kunnen beïnvloeden.
Pre- en probiotica
Probiotica
In de review van Chafen worden vijf studies van hoge kwaliteit beschreven ([4]; [61]; [77]; [78]; [107]) waarin het effect werd onderzocht van het gebruik van probiotica (prenataal en in de neonatale periode). In twee RCT’s ([61]; [107]) werden probiotica in combinatie met borstvoeding onderzocht en in drie studies werden probiotica bestudeerd bij zwangere vrouwen en hun pasgeborenen. Het gebruik van probiotica in de perinatale periode zou geassocieerd kunnen zijn met een beperkte reductie van de cumulatieve incidentie van allergische huidaandoeningen bij kinderen. Deze resultaten dienen met terughoudendheid geïnterpreteerd te worden, want de trials met de meest significante resultaten gebruikten probiotica in combinatie met borstvoeding, hypoallergene voeding of beide. Hierdoor kon het afzonderlijke effect van probiotica niet worden vastgesteld. De methodologische kwaliteit van de vijf trials was hoog. De update van de literatuur leverde één RCT (n = 189) op van goede kwaliteit bij gezonde kinderen ([137]). De kinderen kregen granen met of zonder Lactobacillus F19 tussen de leeftijd van 4 tot 13 maanden. De cumulatieve incidentie van constitutioneel eczeem op de leeftijd van 13 maanden was 11% (95% BI 4-17%) in de probioticagroep in vergelijking met 22% (95% BI 13-31%) in de placebogroep (p < 0,05).
Prebiotica
In de review van Van der Aa ([131]) werd een RCT ([87]) gevonden van matige kwaliteit (o.a. ‘loss to follow-up’ > 20%) waarin de effecten van prebiotica werden beschreven. In deze studie werden 259 hoogrisicokinderen ingesloten. De interventie bestond uit een gehydrolyseerde eiwitformule met een mix van galacto-oligosachariden en fructo-oligosachariden of een placebo (maltodextrine) voor de duur van 6 maanden. De incidentie van atopische dermatitis was significant lager in de interventietroep vergeleken met in de controlegroep (9,8% vs. 23,1%). Op de leeftijd van twee jaar was de cumulatieve incidentie van atopie nog steeds significant verlaagd. Ondanks de veelbelovende resultaten zijn de auteurs terughoudend in hun conclusie vanwege het hoge percentage ‘loss to follow-up’.
3.1.4 Bijwerkingen en complicaties van de interventies
Om een goede afweging te maken tussen de voor- en nadelen van een interventie is het van belang informatie te hebben over de mogelijke bijwerkingen en complicaties van interventies. Er zijn echter geen gegevens gevonden over de mogelijke bijwerkingen van de onderzochte interventies.
Overige overwegingen
Het blijkt dat er weinig gegevens beschikbaar zijn met betrekking tot de universele, selectieve en geïndiceerde preventie van voedselallergie. De werkgroep heeft getracht op basis van onderstaande overwegingen toch tot aanbevelingen te komen voor deze onderwerpen.
Een groot probleem bij de beoordeling van de resultaten uit de diverse studies is de onduidelijkheid over de criteria voor laag- en hoogrisicogroepen en de mate van hydrolyse van de dieetvoedingen.
De studies waarbij borstvoeding (alleen of in combinatie met andere maatregelen) werd onderzocht hebben alle een beperkte methodologische kwaliteit en geven tegenstrijdige resultaten. Dit is in overeenstemming met de resultaten van de NHG-Standaard Voedselovergevoeligheid [159]. Deze tegenstrijdige resultaten kunnen samenhangen met een aantal factoren: het betreffen veelal retrospectieve studies, het opzetten van een RCT van goede kwaliteit is met borstvoeding niet mogelijk en er treedt bias op door de samenstelling van de onderzoeksgroepen (deelnemende moeders met een allergische achtergrond zijn veelal oververtegenwoordigd doordat zij beter gemotiveerd zijn). Algemeen wordt aangenomen dat borstvoeding de beste voeding is voor kinderen gedurende de eerste 4-6 maanden, dit is ook op basis van vele andere redenen waarom borstvoeding wordt geadviseerd.
De werkgroep sluit aan bij het advies om bij voorkeur borstvoeding te geven, ondanks een – nog onvoldoende aangetoond – effect op de preventie van voedselallergie. Mogelijk geldt een eventueel preventief effect alleen voor bepaalde subgroepen (bv. genetische factoren en wisselende voedingspatronen waardoor wisselende samenstelling van de borstvoeding) die tot op heden nog niet geanalyseerd zijn.
Voor de hydrolysaten wordt in de diverse studies een positief effect gezien ten opzichte van niet-gehydrolyseerde kunstvoeding op basis van koemelk en soja. Echter de mate van hydrolyse en het soort hydrolysaat (partieel/intensief/wei-eiwit/caseïne) zijn onduidelijk, waardoor de kwaliteit van het bewijs laag is. Op basis hiervan kan het gebruik van hydrolysaten ter vervanging van borstvoeding niet algemeen worden aanbevolen.
Ten aanzien van de introductie van bijvoeding gaat men uit van het concept van het bestaan van een windowfase tussen de 4 en 6 maanden waarin tolerantie gaat ontstaan ([122]; [144]; [94]). Uitstel van introductie van bijvoeding had geen preventief effect maar veelal juist een verhoogd risico op allergieën, waardoor het advies is – ook voor de hoogrisicogroep – om bijvoeding vanaf 4 maanden te introduceren ([113]; [130]; [142]; [143]). Sausenthaler et al. analyseerden twee geboortecohortonderzoeken (GINIplus en LISAplus) in Duitsland met in totaal 9088 kinderen ([113]). Een subgroep van 2252 kinderen met een positieve familieanamnese voor atopie participeerde in een dubbelblind gerandomiseerd onderzoek naar het effect van het tijdstip van introductie van bijvoeding op het ontstaan van allergieën. In deze studies hadden late introductie van bijvoeding en het vermijden van sterk allergene voeding in het eerste levensjaar geen preventief effect op het ontwikkelen van allergieën ([113]). Studies over (pinda-)allergie suggereren dat het strikt vermijden van een allergeen (pinda) sensibiliserend zou kunnen werken. Du Toit et al. vonden dat kinderen van joodse afkomst in Engeland een 10 keer verhoogde kans op pinda-allergie hadden vergeleken met joodse kinderen in Israël. Dit verschil kon niet verklaard worden door een verschil in atopie, sociale klasse of genetische achtergrond. Het is opvallend dat kinderen in Israël al vroeg beginnen met het consumeren van pinda’s, terwijl in Engeland pinda’s het eerste jaar vermeden worden ([36]).
Dit advies om vanaf 4 maanden met bijvoeding te starten is in tegenspraak met het advies van de World Health Organization (WHO) om 6 maanden exclusieve borstvoeding te geven. Het advies van de WHO wordt echter gegeven met het oog op het risico op ondervoeding en infecties bij jonge kinderen in ontwikkelingslanden en niet ter preventie van voedselallergie.
Voor het effect van probiotica perinataal werden studies van hoge kwaliteit gezien die matig bewijs leveren voor een beperkte reductie van allergische huidaandoeningen. Het effect van exclusief probiotica is veelal in combinatie met andere maatregelen bestudeerd (borstvoeding, hydrolysaten). Er werden vooralsnog geen overtuigende effecten aangetoond van pre- en probiotica bij de preventie van allergieën.
Er zal nog veel onderzoek gedaan moeten worden met een goede opzet en uitvoering om de vele vragen te beantwoorden rond voedselallergie en de preventie ervan.
Ouders zijn, vooral na eerdere ervaringen, erg gemotiveerd om preventieve maatregelen te nemen. Met de huidige onduidelijke/beperkte evidence is het van groot belang ouders de juiste informatie te geven, zodat ze de te leveren inspanning (inclusief kosten) en het beperkte/nog onvoldoende bekende effect tegen elkaar kunnen afwegen. Mogelijk geven de preventieve maatregelen alleen een positief tijdelijk effect/uitstel van de allergische symptomen, hetgeen voor ouder en kind ook de moeite waard kan zijn.
De Gezondheidsraad gaf in 2007 het advies niet af te stappen van de huidige adviezen ter preventie van voedselallergie totdat er betere vormen van preventie beschikbaar zijn ([154]). Na 2007 is er toenemende evidence gekomen dat het introduceren van bijvoeding na de zesde maand niet effectief en mogelijk zelfs schadelijk is, zodat het zinvol is dit advies te herzien en de introductie van bijvoeding te adviseren vanaf de leeftijd van 4 maanden. Tevens is het van belang het gebruik van hydrolysaten niet algemeen te adviseren.
Afstemming tussen de eerste, tweede en derde lijn van de adviezen rond de preventie van voedselallergie is voor ouders van veel belang voor de geloofwaardigheid van de adviezen en het opvolgen ervan. Een recente review door Nederlandse auteurs geeft de huidige stand van zaken rond preventie van voedselallergie goed weer ([76]).
3.1.5 Verwijzen bij koemelkallergie
Kinderen met koemelkallergie zonder ernstige symptomen kunnen binnen de JGZ gediagnosticeerd en behandeld worden, mits financiering voor uitvoering van de DBPGVP aan de JGZ gerealiseerd is. Daar wordt momenteel aan gewerkt. Tot die tijd worden kinderen doorverwezen naar de kinderarts.
Kinderen met ernstige symptomen na inname van koemelk worden verwezen naar de huisarts/kinderarts Dit geldt voor kinderen die/met:
- een anafylactische reactie (Muellerstadium 3-4) op koemelk hebben doorgemaakt;
- astma; omdat de diagnose astma niet goed is te stellen op jonge leeftijd geldt dit ook voor jonge kinderen met perioden van bronchusobstructie, waarvoor regelmatig of recent medicatiegebruik;
- gereageerd hebben op een kleine hoeveelheid koemelk;
- ernstige reacties op borstvoeding (consensus);
- toename in ernst van de reacties in de tijd;
- ouder dan 5 jaar zijn.
Ook worden verwezen:
- kinderen ouder dan 1 jaar voor de eerste diagnosestelling;
- kinderen met onduidelijke symptomen.
In het diagnostische proces van koemelkallergie kan de hulp van de diëtist op verschillende momenten worden ingeroepen: bij het afnemen van een voedingsanamnese (bij oudere kinderen) en bij het adviseren van een diagnostisch of therapeutisch koemelkvrij dieet. Het volledig vermijden van koemelk is essentieel in de diagnostische fase om de klachten te doen verminderen of te doen verdwijnen. Er zijn geen studies bekend die de waarde van de dieetanamnese bij een vermoeden van koemelkallergie hebben onderzocht ([151]). Bij jonge flesgevoede kinderen is de dieetanamnese nog relatief gemakkelijk omdat zij nog weinig (samengestelde) voedingsmiddelen gebruiken. Bij deze kinderen is de deskundigheid van de diëtist voor het afnemen van een anamnese meestal niet nodig. Zodra het kind ouder is en bijvoeding gaat gebruiken of al een uitgebreid dieet gebruikt met samengestelde producten, is begeleiding door een diëtist voor het samenstellen van een koemelkvrij dieet aanbevolen. De diëtist kan de introductie van bijvoeding aanmoedigen. Hiermee wordt voorkomen dat de bijvoeding onnodig wordt beperkt, worden dieetfouten voorkomen, wordt gezorgd voor een volwaardige voeding en kan/kunnen het kind/de ouder(s) bij de diëtist terecht met vragen over de uitvoerbaarheid van het dieet ([42]; [163]). In de therapeutische fase kan worden bekeken of kleine hoeveelheden melk verwerkt in producten worden verdragen. Hiervoor is verwijzing naar een diëtist, bij voorkeur iemand met specifieke deskundigheid in allergie, nodig.
Voor zogende moeders geldt dat zij bij vermoeden van een koemelkallergie bij hun kind een koemelkvrij dieet moeten volgen ([42]). Soms worden kleine hoeveelheden melk verwerkt in producten nog wel verdragen (consensus), maar in de diagnostische fase wordt volledige eliminatie nagestreefd. Een koemelkvrij dieet kan gemakkelijk leiden tot tekorten in onder andere energie, calcium en vitamine B2 bij zowel de moeder als het kind zelf, waardoor de borstvoeding kan teruglopen of de moeder ongewenst gewicht verliest. Voor haar is begeleiding door een diëtist bij een koemelkvrij dieet aan te bevelen als het dieet langer dan 4 weken wordt gevolgd, als zij ongewenst gewicht verliest of bij vragen over of problemen met het dieet. Hierbij moeten andere begeleidende maatregelen om de borstvoeding op gang te houden niet worden vergeten. Zuivelproducten kunnen niet worden vervangen door sojaproducten in de diagnostische fase (consensus), maar kunnen wel in de therapeutische fase door de moeder worden gebruikt. Bijna alle kinderen met koemelkallergie zijn door kruisreactiviteit ook allergisch voor geiten- (89-100%) en schapenmelk, deze producten worden daarom afgeraden. Dit geldt ook maar in mindere mate voor kamelen- (25%), paarden- (4%) en ezelmelk (4-17%) ([42]; [69]). Bij blijvende klachten wordt verwezen naar de tweede lijn.
3.1.6 Koemelkvrij dieet
Achtergrond
Bij het vermoeden van koemelkallergie moeten in de diagnostische fase alle producten met koemelk volledig worden vermeden om te zien of de klachten verminderen. Een sterke afname van de klachten is een mogelijke aanwijzing voor de aanwezigheid van koemelkallergie. Als de klachten niet afnemen kan koemelk weer worden geïntroduceerd in het dieet. Als de klachten afnemen kan er sprake van koemelkallergie zijn. Om de diagnose koemelkallergie te stellen moet verder onderzoek verricht worden. Het is van belang om de juiste diagnose te stellen, omdat eliminatiediëten nadelige effecten kunnen hebben, zoals afbuigende groei, een stagnerende introductie van bijvoeding, fixatie op voedsel als oorzaak van onschuldige symptomen, sociale isolatie en impact op de kwaliteit van leven ([5]; [24]; [26]; [89]; [111]).
Voeding tijdens de diagnostische fase van koemelkallergie
Tijdens een koemelkvrij dieet bij jonge kinderen die standaardkunstvoeding op basis van koemelk gebruiken moet de voeding vervangen worden door een volwaardige hypoallergene kunstvoeding. Alleen hypoallergene kunstvoedingen die door ten minste 90% van de kinderen verdragen worden komen hiervoor in aanmerking (Anonymous, 2000; [24]). Dit zijn intensief gehydrolyseerde kunstvoedingen (eHF), ook wel eiwithydrolysaten genoemd, en kunstvoedingen op basis van vrije aminozuren (AA). In Nederland zijn de volgende kunstvoedingen verkrijgbaar, die gebruikt kunnen worden bij een koemelkvrij dieet:
- intensief gehydrolyseerde kunstvoeding op wei-eiwit basis (eHF-W);
- intensief gehydrolyseerde kunstvoeding op caseïnebasis (eHF-C);
- kunstvoeding op basis van vrije aminozuren (AA);
- kunstvoeding op basis van soja (SF).
1. Intensief gehydrolyseerde kunstvoeding of voeding op basis van aminozuren?
Hoewel er op basis van de huidige literatuur geen aanbevelingen kunnen worden gedaan voor de keuze tussen eHF en AA, zijn er in sommige studies allergische reacties op eHF beschreven ([26]; [111]). De DRACMA beveelt voor IgE-gemedieerde koemelkallergie het gebruik van AA aan voor kinderen die anafylactisch hebben gereageerd op koemelk en die op het moment van aanbeveling (nog) geen eHF gebruiken (lage kwaliteit van bewijs) ([26]; [74]; [111]). Bij de overige kinderen met IgE-gemedieerde koemelkallergie wordt een eHF aanbevolen. De werkgroep sluit zich niet aan bij het advies van de DRACMA om bij kinderen met anafylaxie per definitie een AA te adviseren, omdat anafylactische reacties op eHF zeldzaam zijn. Wel acht de werkgroep het aan te bevelen dat bij een anafylactische reactie op koemelk, waarbij het kind nog geen eHF gebruikt, de eHF klinisch wordt geïntroduceerd. Bij de werkgroep bestaat de klinische indruk dat bij een beperkte groep kinderen met koemelkallergie (zowel met directe als vertraagde reacties op koemelk) eHF onvoldoende effectief is. Bij deze kinderen nemen de klachten in de diagnostische fase onvoldoende af bij gebruik van eHF of blijft de groei achter (consensus), terwijl er toch een sterk vermoeden is van koemelkallergie. Bij deze beperkte groep kinderen kan, uitsluitend in de tweede of derde lijn, in de diagnostische fase eHF worden vervangen door AA, aanvankelijk voor een proefperiode van maximaal enkele maanden.
In de dagelijkse praktijk wordt tijdens de diagnostische fase vaak gewisseld tussen eHF-W, eHF-C en AA als klachtenafname niet snel genoeg optreedt. Meestal wordt eerst eHF-W, vervolgens eHF-C en ten slotte AA geadviseerd, omdat in de eerste lijn op basis van de huidige richtlijnen alleen eHF-W wordt geadviseerd, omdat bij sommige hulpverleners de klinische indruk bestaat dat eHF-C mogelijk effectiever is dan eHF-W of omdat ouders of hulpverleners vanwege de lagere kosten beginnen met eHF-W. Uit de literatuur zijn geen vergelijkende studies tussen eHF-C en eHF-W bekend, dus een aanbeveling over de keuze tussen eHF-C of eHF-W kan niet worden gegeven. Wel zijn gegevens over de peptidegrootte van de diverse voedingen beschikbaar. Alle eHF-voedingen bevatten uitsluitend peptiden van < 3000 dalton, maar de peptiden van de eHF-C zijn gemiddeld iets kleiner dan die van de eHF-W. Het is onbekend of dit leidt tot klinische effecten. Hoewel het verschil in effectiviteit tussen eHF-C en eHF-W bij de behandeling van koemelkallergie een onderwerp van discussie is in Nederland, speelt dit in de internationale literatuur geen rol. Bij sommige leden van de werkgroep bestaat echter de klinische indruk dat bij kinderen met aantoonbaar sIgE eHF-C mogelijk effectiever is dan eHF-W. Het (te vaak) wisselen tussen eHF-C en eHF-W is niet wenselijk. Dit kan worden voorkomen door het effect van de eHF goed te evalueren, samen met de ouders. eHF-W is goedkoper dan eHF-C. Dit kan mogelijk een rol spelen bij de keuze van het type eHF.
Partieel gehydrolyseerde kunstvoedingen (Nutrilon HA, Friso HA, Nutrilon Omneo-Comfort) zijn niet geschikt voor de diagnostiek en behandeling van koemelkallergie ([42]).
2. Intensief gehydrolyseerde voeding of voeding op basis van soja?
De DRACMA stelt dat SF niet onder de leeftijd van 6 maanden gegeven moet worden vanwege mogelijk voedingskundige nadelen. De DRACMA is hierin niet duidelijk. Vermoedelijk wordt dit gesteld naar aanleiding van de studie van Agostoni et al. waarin de groei van kinderen met een SF iets achterbleef vergeleken bij die met een eHF ([5]). Er is slechts één gerandomiseerde studie waarin de prevalentie van soja-allergie bij kinderen met koemelkallergie wordt onderzocht. In een RCT (van matige kwaliteit) van Klemola et al. is de prevalentie van soja-allergie bij kinderen jonger dan 6 maanden significant hoger (25%) dan bij kinderen ouder dan 6 maanden (5%) ([74]). Overgevoeligheid voor SF kwam even vaak voor bij kinderen met en zonder IgE tegen soja. Ook in de follow-upstudie had op de leeftijd van 4 jaar slechts één kind een reactie op soja in een open provocatie met soja. Bovendien waren er geen significante verschillen in sensibilisatie voor soja en pinda’s, noch in gerapporteerde reacties op pinda’s door de ouders ([75]). Ook in een recente cohortstudie in Israël wordt onder kinderen met een IgE-gemedieerde koemelkallergie geen soja-allergie gevonden ([72]). Een mogelijk voordeel van SF zou kunnen zijn dat de smaak minder afwijkend is dan die van eHF en AA. Er bestaan echter nauwelijks studies die verschil in smaakontwikkeling hebben onderzocht tussen kinderen die zijn gevoed met soja of eHF ([85]).
In een position paper van het ESPGHAN Committee on Nutrition wordt gesteld dat kunstvoedingen op basis van soja mogelijk nadelen hebben op de lange termijn vanwege het gehalte aan fytaat, aluminium en fyto-oestrogenen ([5]). Om die reden raadt de ESPGHAN het gebruik van soja onder de leeftijd van 6 maanden af en wordt boven de leeftijd van 6 maanden de voorkeur gegeven aan eHF bij koemelkallergie. Ook door de American Academy of Pediatrics wordt gesteld dat er tot op heden geen conclusies kunnen worden getrokken ten aanzien van de korte- of langetermijneffecten van fyto-oestrogenen ([13]). Voor de discussie zijn de eventuele nadelen van soja en het standpunt van de ESPGHAN voor de werkgroep van doorslaggevende betekenis, ondanks het feit dat de kans op soja-allergie boven de leeftijd van 6 maanden gering lijkt. Om die reden geeft de werkgroep vooralsnog de voorkeur aan eHF boven SF onder de leeftijd van 1 jaar (consensus). Tussen de leeftijd van 6 en 12 maanden acht de werkgroep het wel verantwoord dat sojaproducten in beperkte mate worden gegeven als aanvulling op eHF of AA, bijvoorbeeld in de vorm van sojavla of een sojavariatie op yoghurt (soja-yofu) (consensus).
Kinderen ouder dan 1 jaar die een koemelkvrij dieet moeten gaan volgen en die tot op dat moment standaardkunstvoeding en koemelkproducten hebben gebruikt, weigeren in het algemeen eHF vanwege de bittere smaak. Bij deze kinderen kan in de behandelfase worden overgegaan op calciumverrijkte rijstemelk of sojamelk. Overigens is rijstemelk geen volledige vervanging van melk, omdat het nauwelijks eiwit bevat.
Aanbevelingen
3.1.7 Koemelkprovocatietest: hoe, door wie en randvoorwaarden
Open of dubbelblinde placebogecontroleerde koemelkprovocatietest?
Achtergrond
Voedselprovocaties worden uitgevoerd bij kinderen met een vermoeden van koemelkallergie om de diagnose koemelkallergie te bevestigen of uit te sluiten. Een voedselprovocatie moet worden voorafgegaan door een koemelkvrij dieet gedurende ten minste 4 weken met sterke afname van de symptomen. Tijdens een voedselprovocatietest krijgt het kind onder medisch toezicht koemelk in opklimmende doses toegediend. Het vermoeden van koemelkallergie komt tot stand op basis van (voedings)anamnese, lichamelijk onderzoek én een positief effect van een koemelkvrij dieet. Er zijn twee vormen van voedselprovocatietesten met koemelk.
• Open voedselprovocatietest (OVP). Hierbij krijgt het kind in oplopende doses onder medisch toezicht koemelk toegediend: op locatie, op locatie beginnend en thuis afgemaakt of thuis bij borstvoeding.
• Dubbelblinde placebogecontroleerde voedselprovocatietest (DBPGVP). Hierbij krijgt het kind op locatie in oplopende doses onder medisch toezicht in twee sessies testvoeding met of zonder koemelk toegediend, waarbij noch de betrokken behandelaars noch de ouders (en het kind) op de hoogte zijn wanneer de testvoeding koemelk bevat.
Wat is de diagnostische waarde van de DBPGVP ten opzichte van OVP?
Bij het beantwoorden van deze vraag is uitgegaan van de RAND-working-paper opgesteld voor de recent gepubliceerde Amerikaanse NIAID-richtlijn voor de diagnose en behandeling van voedselallergie, omdat de vraag in dit rapport beantwoord is met behulp van de GRADE-methode ([151]). Aanvullende informatie is verkregen uit de DRACMA en NIAID en een update van de literatuurzoekstrategie van de RAND ([19]; [42]).
Hoewel de DBPGVP door moet gaan voor de gouden standaard zijn er weinig studies die de diagnostische waarde van de OVP ten opzichte van de DBPGVP hebben onderzocht. De DBPGVP wordt niet op grote schaal toegepast door gebrek aan gespecialiseerd personeel, tijd en geld, het risico op anafylaxie en een gebrek aan overeenstemming over de criteria voor een positieve test. Toch is het van groot belang om de diagnose koemelkallergie goed te stellen om foutpositieve diagnoses te voorkomen en zo onnodige eliminatiediëten te voorkomen, evenals deficiënties in het dieet, zorgen en sociale isolatie. Niet-specifieke symptomen zoals huiduitslag kunnen ten onrechte worden toegeschreven aan voedselallergie. Het grootste probleem bij de diagnostiek van voedselallergie is dat er geen eenheid is in de literatuur over diagnostische criteria ([29]).
Samenvattend wordt gesteld dat, hoewel de DBPGVP de gouden standaard is, deze test op veel onderdelen nog niet gevalideerd en gestandaardiseerd is. Er zijn slechts weinig studies over de noodzaak en methodologie van DBPGVP’s. Valkuilen bij het uitvoeren van DBPGVP’s kunnen placeboreacties zijn, de samenstelling van de testvoeding en de vorm waarin het allergene voedingsmiddel is verwerkt in de testvoeding. De kwaliteit van de geïncludeerde studies is matig.
Overige overwegingen
Het grootste voordeel van de DBPGVP ten opzichte van de OVP is dat mogelijke bias (subjectieve, bevooroordeelde waarneming) bij patiënten én betrokken hulpverleners wordt gereduceerd ([19]). Hierdoor is de DBPGVP de meest betrouwbare test. Nadelen van de DBPGVP zijn de lange tijdsduur en hoge kosten ten opzichte van de makkelijker uitvoerbare OVP. Zie voor de gedetailleerde beschrijving van de DBPGVP de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’ van de Nederlandse Vereniging voor Kindergeneeskunde ([166]).
In het rapport ‘Voedselallergie’ van de Gezondheidsraad en in het rapport ‘Diagnostiek van koemelkallergie in Nederland: Anders’ wordt aanbevolen om een makkelijk uitvoerbare DBPGVP te ontwikkelen voor de eerste lijn ([146]; [154]). In de knelpuntenanalyse voorafgaand aan het ontwikkelen van deze richtlijn kwam de behoefte naar voren van JGZ-professionals aan een objectieve test om koemelkallergie te diagnosticeren, zie 9.1 Knelpuntenanalyse.
Een OVP kan worden gebruikt voor het uitsluiten van de diagnose koemelkallergie en voor herevaluatie van de noodzaak van het koemelkvrije dieet na een eerdere positieve DBPGVP.
Voor het doen van sensibilisatieonderzoek kan specifiek IgE tegen koemelk worden bepaald of kan een huidpriktest met koemelk worden uitgevoerd. In de eerste lijn wordt een sIgE-bepaling voor koemelk of een ‘screeningtest voor voedselallergenen’ (een IgE-bepaling voor een mix van voedingsbestanddelen) afgeraden. Bij aantoonbaar sIgE voor koemelk is sensibilisatie aangetoond, maar is het nog niet bewezen dat er een verband bestaat met de symptomen. Anderzijds kan een kind een koemelkallergie hebben zonder aantoonbare sensibilisatie (Anonymous, 2000; [24]; [42]). Over het algemeen zijn sensitiviteit en specificiteit van sIgE en huidpriktest bij koemelkallergie laag (Anonymous, 2000; [24]). Hierdoor bestaat de kans dat bij kinderen met sensibilisatie voor koemelk de diagnose koemelkallergie onterecht alleen op basis van sensibilisatieonderzoek wordt gesteld.
Waar kunnen voedselprovocatietesten het beste worden uitgevoerd?
Er is geen systematische review bekend op basis waarvan deze vraag beantwoord kan worden. De aanbevelingen berusten op een aantal internationale en nationale publicaties en consensus binnen de werkgroep.
Veiligheid
Bij het uitvoeren van voedselprovocatieonderzoek staat veiligheid voorop. Dat betekent dat ernstige reacties moeten worden voorkomen en – als zij onverhoopt toch optreden – adequaat moeten kunnen worden opgevangen (Anonymous, 2000; [24]; [42]). Tot ernstige reacties worden luchtweg- en cardiovasculaire symptomen gerekend (Anonymous, 2000; [57]). Het is niet goed mogelijk om de ernst van een allergische reactie te voorspellen. Wel zijn er verschillende risicofactoren die de kans op een ernstige reactie kunnen vergroten (Anonymous, 2000; [24]; [64]; [89]; [90]).
- Ernstige (anafylactische) reactie.
- Instabiel astma of ernstig astma.
- Toename van de ernst van de reacties in de tijd.
- Eerdere reactie op een kleine hoeveelheid koemelk.
- Leeftijd ouder dan 5 jaar. Een dodelijke afloop bij voedselallergie is vooral beschreven bij kinderen ouder dan 5 jaar.
De genoemde risicofactoren zijn ontleend aan observationele studies naar (bijna) fatale reacties bij voedselallergie in het dagelijkse leven ([102]; [104]; [105]). Een paar studies hebben onderzoek gedaan naar de veiligheid van voedselprovocaties ([16]; [67]; [169]). Hieruit blijkt dat voedselprovocaties, mits door ervaren mensen verricht, veilig kunnen worden uitgevoerd. James et al. bestudeerden in 1994 in een derdelijnscentrum DBPGVP-testen bij 320 kinderen en volwassenen (leeftijd 0,5-30 jaar, mediane leeftijd 4,4 jaar) met constitutioneel eczeem ([67]). 59% van de 205 patiënten met een positieve test ontwikkelde luchtwegsymptomen. Slechts 7% had een daling van de longfunctie (FEV1) van meer dan 20%. De symptomen die Perry et al. vonden bij 584 kinderen die een DBPGVP hadden ondergaan in een tweede-/derdelijnscentrum waren alle behandelbaar met kortwerkende antihistaminica, adrenaline, beta-antagonisten of corticosteroïden ([102]). Er traden geen cardiovasculaire symptomen op en ziekenhuisopname was niet nodig.
In de literatuur wordt aangegeven dat voedselprovocaties onder medisch toezicht moeten plaatsvinden. Verlengde voedselprovocaties, waarbij een milde vertraagde reactie op herhaalde doses wordt verwacht, kunnen ook thuis worden uitgevoerd ([42]; [92]). De DRACMA geeft aan dat alleen bij afwezigheid van sensibilisatie een verlengde provocatie thuis kan plaatsvinden ([42]). Laagrisicoprovocaties kunnen ook in een praktijksetting van een arts worden uitgevoerd en worden in de Amerikaanse literatuur geduid als ‘office challenges’ ([42]; [92]). Dit laatste is ook afhankelijk van de ervaring van de superviserende arts en zijn/ haar staf. Hoogrisicoprovocaties moeten in het ziekenhuis plaatsvinden ([92]). Voor de Nederlandse situatie is de zogenaamde office challenge vergelijkbaar met een praktijksituatie in de JGZ- en de huisartsenpraktijk, met dit verschil dat in de VS meestal vrijgevestigde specialisten (kinderartsen of allergologen) de voedselprovocaties uitvoeren.
Situatie in Nederland
Uit de knelpuntanalyse van de JGZ komt naar voren dat het thuis uitvoeren van een OVP als knelpunt wordt ervaren omdat reacties niet geobjectiveerd kunnen worden. De NHG-Standaard Voedselovergevoeligheid uit 2010 geeft aan dat een OVP met koemelk in de huisartsenpraktijk uitgevoerd kan worden, behalve bij een doorgemaakte ernstige reactie, louter subjectieve reacties of ernstig therapieresistent constitutioneel eczeem ([159]; [161]).
De werkgroep is verdeeld over de vraag waar de OVP (als ‘second best’ test) moet worden uitgevoerd als een DBPGVP niet mogelijk is: geheel op locatie (JGZ) binnen een tijdsbestek van enkele uren of met de huidige methode waarbij de eerste dosis in de JGZ wordt verstrekt en de rest van de provocatie uitgesmeerd over een paar dagen in de thuissituatie wordt verricht. Hierbij gelden de volgende randvoorwaarden: de symptomen worden thuis geregistreerd, de provocatie wordt niet door de ouders zonder overleg met de arts afgebroken en de ouders komen terug voor objectivering van symptomen.
Nadelen van het uitvoeren van een OVP die thuis wordt afgemaakt zijn: kans op ernstige reacties thuis bij verkeerde indicatiestelling voor thuisprovocatie, geen observatiemogelijkheden waardoor de interpretatie van de symptomen bij de ouders wordt gelegd, het risico van het eigenhandig staken van de provocatie door de ouders en het risico van verwatering van randvoorwaarden voor het goed uitvoeren van de OVP thuis.
De werkgroep is van mening dat de locatie waar de provocatie kan worden uitgevoerd ten eerste wordt bepaald door het risico op (ernstige) reacties van het kind en de mogelijkheid om eventuele ernstige reacties adequaat te kunnen behandelen ([151]; [92]). Daarnaast spelen praktische aspecten een rol, zoals de mogelijkheid om testvoeding te bereiden, expertise van het personeel en de mogelijkheid de patiënt te observeren en adequaat te kunnen behandelen ([92]). Ook moeten er goede afspraken gemaakt worden tussen JGZ, huisarts en spoedeisende hulp waar de patiënt kan worden gezien indien er vertraagde reacties zijn.
Op grond van het bovenstaande kan voor de Nederlandse situatie worden geconcludeerd dat hoogrisico-DBPGVP’s en hoogrisico-OVP’s met koemelk voorbehouden zijn aan ervaren tweede- en derdelijnscentra. Laagrisicoprovocaties met koemelk kunnen in de eerste, tweede en derde lijn plaatsvinden. Laagrisico-DBPGVP’s moeten volledig op locatie worden uitgevoerd. Laagrisico-OVP’s (als ‘second best tests’) in de eerste lijn kunnen zowel volledig op locatie als ten dele thuis worden uitgevoerd.
Randvoorwaarden
Bij provocatie in de JGZ moet aan de volgende voorwaarden worden voldaan ([151]; [92]):
1. Ervaren personeel
Het kind moet adequaat kunnen worden behandeld bij het optreden van allergische reacties. Hiervoor is het nodig dat de JGZ-professionals geschoold worden in het verrichten van provocaties en het vroegtijdig herkennen van (ernstige) reacties en er in de JGZ antihistaminica en adrenaline(auto)injectoren beschikbaar komen. Goede monitoring en protocollaire afspraken omtrent het toedienen van medicatie (antihistaminica en/of adrenaline i.m.) zijn noodzakelijk. Overleg met de Inspectie voor de Gezondheidszorg is nodig. Bovendien is multidisciplinaire samenwerking tussen jeugdartsen, jeugdverpleegkundigen, verpleegkundig specialisten en diëtisten nodig.
2. Observatie tot 2 uur na de laatste dosis
In de JGZ kan aan deze voorwaarde in de huidige situatie niet of nauwelijks worden voldaan vanwege de beperkte openingstijden. De openingstijden zouden aangepast moeten worden. Voor jonge kinderen die tussendoor slapen kan de wachtruimte te vol en te druk zijn.
3. Adequate honorering van voedselprovocatietesten
Hiervoor zal overleg gevoerd moeten worden met de zorgverzekeraars. Enerzijds kost het uitvoeren van voedselprovocatietesten geld, anderzijds kan door het uitvoeren van provocatieonderzoek de instroom naar de tweede en derde lijn worden beperkt. Ook wordt met het terugdringen van foutpositieve diagnostiek van koemelkallergie onnodig gebruik van het duurdere eHF voorkomen.
4. Testvoeding
Voor het gemakkelijk en snel bereiden van de testvoeding op basis van intensief gehydrolyseerde voeding zullen naar verwachting speciale gestandaardiseerde en gevalideerde provocatiekits met alle gangbare intensief gehydrolyseerde kunstvoedingen binnenkort beschikbaar komen. Deze provocatiekits bestaan uit zakjes met poeder voor zowel de placeboprovocatie als de verumprovocatie die alleen hoeven worden aangelengd met water.
5. Nauwe samenwerking met de huisarts
De huisarts wordt geïnformeerd wanneer de koemelkprovocatie gaat plaatsvinden. Er zijn lokale afspraken nodig over wie het kind bij late reacties, met name buiten ‘kantooruren’, beoordeelt: jeugdarts, huisarts, kinderarts of arts van de spoedeisende hulp.
Aanbevelingen
3.2 Coeliakie
Coeliakie is een ziekte waarbij naast genetische componenten (HLA en non-HLA) ook omgevingsfactoren, met name de inname van gluten, een rol spelen.
Of de verschijnselen van coeliakie bij een belastend genenpatroon optreden, is tot op heden nog niet voorspelbaar. Het tijdstip en de wijze van glutenintroductie in de voeding van zuigelingen zouden effect kunnen hebben op het tijdstip van optreden van de verschijnselen en op de ernst van de verschijnselen en mogelijk zelfs het ontstaan van de ziekte kunnen voorkomen.
Onderzoeken bij zuigelingen zonder belaste familieanamnese zijn geanalyseerd op effecten van preventieve interventies. Er is specifiek gekeken naar het effect van borstvoeding en het effect van introductie van gluten tijdens borstvoeding.
Aanbevelingen
3.2.1 Signaleren van coeliakie
Coeliakie is een frequent (1:100-200) voorkomende aandoening die momenteel bij een minderheid van de patiënten (1:600-1000) wordt gediagnosticeerd. Vermoedelijk ligt de drempel voor diagnostiek eerder te hoog dan te laag. Een belangrijke oorzaak is de grote spreiding in ernst en variatie van de klachten. Bij het literatuuronderzoek werd een beperkt aantal meta-analyses en systematische reviews gevonden, met als gemeenschappelijk kenmerk dat de studies waarop de conclusies waren gebaseerd grote heterogeniteit vertoonden en over het algemeen een laag bewijsniveau hadden. De hiernavolgende conclusies moeten in dat licht worden gezien.
Dieetgegevens. Coeliakie ontstaat pas na de introductie van gluten in de voeding. De aandoening moet dus alleen in de differentiaaldiagnose worden opgenomen van kinderen (en volwassenen) bij wie gluten in de voeding is geïntroduceerd. Voor betrouwbare diagnostiek is het bovendien nodig dat de betreffende persoon nog steeds glutenbevattende voeding gebruikt.
Symptomen. Uit de tabellen (zie Klachten en symptomen bij volwassenen) blijkt dat bij vrijwel alle maag-darmsymptomen waarvoor geen andere verklaring wordt gevonden, aan coeliakie moet worden gedacht. Van de functionele maag-darmklachten geldt dat in elk geval voor het prikkelbaredarmsyndroom bij volwassenen.
Daarnaast zijn ook tandglazuurdefecten, ijzergebreksanemie, onbegrepen botbreuken en osteoporose, problemen met lengte en gewicht en persisterende vermoeidheid redenen voor coeliakiescreening. Betreffende neurologische aandoeningen zijn er onvoldoende aanwijzingen voor een relatie met coeliakie, met de mogelijke uitzondering van epilepsie met intracerebrale calcificaties. Van de laboratoriumbevindingen geldt een mogelijke relatie met coeliakie voor onbegrepen (ijzergebreks)anemie en hypertransaminasemie.
Dermatitis herpetiformis. Dit wordt ook wel ‘coeliakie van de huid’ genoemd. Hoewel zeldzaam bij volwassenen en extreem zeldzaam bij kinderen is het van groot belang om de aandoening te herkennen; hiervoor is een biopsie uit de niet-aangedane huid naast een laesie essentieel. In het biopt (met IgA-depots) kunnen neerslagen van transglutaminase-antilichamen worden gevonden. Bij dermatitis herpetiformis moet altijd coeliakiediagnostiek worden ingezet.
Andere afwijkingen. Hoewel alle auto-immuunziekten een zekere band hebben met coeliakie, staat alleen voor diabetes mellitus type 1 vast dat coeliakiescreening zinvol is. Daarnaast lijkt het verstandig om ook bij de (zeldzame) auto-immuunziekten van de lever eenmalig coeliakiescreening te verrichten. Daarnaast zijn er enkele syndromen met een verhoogd coeliakierisico; hoewel het bewijs mager is, geldt voor het Downsyndroom en vermoedelijk ook voor het syndroom van Williams en het syndroom van Turner dat coeliakiescreening van waarde kan zijn.
Eerstegraadsfamilieleden. De sterke familiaire associatie van coeliakie maakt screening bij broers en zussen, kinderen en ouders zinvol. Voor de kinderen in deze groep geldt dat nog sterker, omdat zij nog geen eigen keuzes kunnen maken en nog in de groei zijn.
Zie ook Klachten en symptomen bij volwassenen.
3.2.2 Coeliakiediagnostiek
Deze bestaat uit informatie over de genetische achtergrond (DQ2, DQ8), serologische screening (IgA- en bij selectieve IgA-deficiëntie IgG-antilichamen tegen endomysium (EmA), transglutaminase type 2 (TG2A) en eventueel gedeamineerde glutenpeptiden (DGPA)) en histologische bevestiging (dunnedarmbiopten). Onder strikt vastgelegde omstandigheden kunnen bij een klein deel van de kinderen met verdenking van coeliakie de dunnedarmbiopten achterwege worden gelaten. Coeliakiediagnostiek heeft alleen maar zin nadat gluten in de voeding is geïntroduceerd en is alleen maar betrouwbaar zolang als de voeding voldoende gluten bevat. Dit geldt niet voor DQ2- en DQ8-bepaling, maar deze hebben meer waarde bij het uitsluiten van de diagnose dan bij de bevestiging ervan ([60]).
3.2.3 Effecten van borstvoeding
Borstvoeding versus geen borstvoeding
Er waren niet genoeg data voorhanden om bovenstaande vergelijking te maken.
Duur van de borstvoeding
Er was te veel heterogeniteit in de wijze waarop de duur van het geven van borstvoeding was gemeten (variërend van 0 dagen tot 2 maanden, vergelijkingen tussen > 1 of 2 maand(en) en < 1 of 2 maand(en) borstvoeding). Uit de resultaten van de individuele studies lijkt er een tendens te bestaan voor een beschermend effect van een langere duur van borstvoeding op het ontstaan van coeliakie.
Borstvoeding op het moment van introductie van gluten
Vier studies (n = 1969; 714 cases, 1255 controles) leverden voldoende data ([8]; [39]; [65]; [103]) voor een meta-analyse om kinderen die wel of geen borstvoeding kregen op het moment dat gluten werden geïntroduceerd in de voeding te vergelijken ([6]). Het risico op coeliakie was significant lager voor kinderen die borstvoeding ontvingen op het moment dat gluten werden geïntroduceerd (OR 0,48; 95% BI 0,40 – 0,59). In een meta-analyse zou zowel vroege (≤ 4 maanden) als late (≥ 7 maanden) introductie van gluten het risico op coeliakie verhogen ([127]).
Beperkingen van de studies
Er is een aantal beperkingen van de ingesloten studies. Alle studies waren patiëntcontroleonderzoeken die blootstaan aan recall bias. Hierdoor is misclassificatie van de duur van borstvoeding en de leeftijd waarop gluten werden geïntroduceerd mogelijk, wat een overschatting kan veroorzaken van het effect. Een ander gevaar is dat belangrijke confounders die niet gemeten zijn (zoals sociaal-economische status of een positieve familieanamnese) niet gelijk zijn verdeeld over de groepen.
Bijwerkingen en complicaties van de interventies
Om een goede afweging te kunnen maken tussen de voor- en nadelen van een interventie is het van belang informatie te hebben over de mogelijke bijwerkingen en complicaties van interventies. Er zijn echter geen gegevens gevonden over de mogelijke bijwerkingen van de onderzochte interventies.
Overige overwegingen
Borstvoeding heeft afgezien van haar effecten op het ontstaan van coeliakie bewezen gezondheidsvoordelen voor zuigelingen, zowel op de korte als op de langere termijn. Introductie van gluten, in opklimmende hoeveelheden, tijdens de borstvoedingsperiode lijkt een positief effect te hebben op het later/minder optreden van de verschijnselen van coeliakie. De resultaten van onderzoek zijn echter nog te omstreden, zowel wat betreft opzet en methode als uitkomst van de studies, om hier gerechtvaardigd algemene preventieve adviezen voor kunstvoeding op te baseren.
3.2.4 Klachten en symptomen bij volwassenen
Ter informatie volgen hier de symptomen van coeliakie bij volwassenen.
Buikklachten bij volwassenen
Van der Windt et al. constateerden dat de aanwezigheid van uiteenlopende maag-darmklachten over het algemeen een slechte voorspeller was van de kans op coeliakie in de eerste lijn ([132]). Bovendien bleek de bruikbaarheid van de meest betrouwbare tests, EmA en TG2A, in de eerste lijn niet goed te zijn onderzocht. Ford et al. onderzochten in twee meta-analyses het risico van coeliakie bij patiënten met dyspepsie en met prikkelbaredarmsyndroom (PDS) ([44]; [43]). Weliswaar bleek coeliakie vaker voor te komen bij dyspepsiepatiënten (3,2%) dan in de controlegroepen (1,3%), maar het verschil was niet significant ([44]). Bij PDS-patiënten bleek de kans op coeliakie het viervoudige te zijn van die bij personen uit de controlegroepen ([43]). In een oudere studie naar het nut van aanvullend onderzoek bij PDS-patiënten bleek de prevalentie van coeliakie het tienvoudige te zijn van die bij controlegroepen; aanvullend onderzoek naar het nut van serologisch onderzoek bij deze groep werd aanbevolen ([28]; [43]).
Orale pathologie
In een meta-analyse van Giuca et al., verschenen in het Italiaans en alleen in abstract beschikbaar, wordt gesteld dat er genoeg wetenschappelijk bewijs is voor een relatie tussen orale pathologie en coeliakie en dat tandartsen zich hiervan moeten vergewissen ([46]). Een, eveneens Italiaans, gestructureerd review komt tot de conclusie dat tandglazuurafwijkingen significant vaker voorkomen bij coeliakiepatiënten (tot 100%) en dat bij hen dus coeliakiescreening moet plaatsvinden onafhankelijk van de aanwezigheid van gastro-intestinale symptomen. Hoewel geen significante verschillen werden gevonden tussen controlegroepen en coeliakiepatiënten wat betreft aften en idiopathische atrofische glossitis, bevelen zij bovendien aan dat daarbij algemeen lichamelijk onderzoek, eventueel aangevuld met coeliakiescreening, wordt verricht ([99]).
Neurologische afwijkingen
Grossmann voerde een kritische analyse uit van de gepubliceerde evidence voor een relatie tussen coeliakie en neurologische syndromen ([50]). Hij concludeerde dar er een mogelijke relatie was met ataxie (‘gluten ataxia’) en met perifere neuropathie, maar dat het bewijs mager en tegenstrijdig was en dat er geen causaliteit was aangetoond. Vermoedelijk bestaat er wel een (zeldzaam) specifiek syndroom van coeliakie met epilepsie en hersenverkalkingen. Ongeveer dezelfde conclusies worden getrokken in een narratieve review van Pengiran Tengah et al. ([101]).
Leverwaardenstoornissen
Sainsbury et al. voerden een meta-analyse uit naar coeliakie bij cryptogene hypertransaminasemie ([109]). Zij vonden een prevalentie van bewezen coeliakie van 4% (95%-betrouwbaarheidsinterval 1-7%), terwijl hypertransaminasemie werd gevonden bij 27% (13-44%) van de nieuw gediagnosticeerde coeliakiepatiënten. Zij concludeerden dat een onbegrepen stijging van ASAT en ALAT zou moeten leiden tot coeliakiescreening. Mirzaagha et al. onderzochten de gepubliceerde prevalentie van coeliakie bij patiënten met auto-immuunleverziekten ([86]). Hoewel het overzicht suggereert dat de prevalentie verhoogd is, zijn de data incompleet en in veel gevallen ontbreekt histologisch onderzoek; dit verhindert een harde conclusie.
Botafwijkingen
Onbehandelde coeliakie gaat bij volwassenen vaak gepaard met verminderde botdichtheid. Er is echter geen meta-analyse of systematische review die deze relatie analyseert. Bianch en Bardella geven in een klinische review het advies om coeliakiescreening te verrichten bij patiënten met botbreuken die onverwacht of onverwacht ernstig zijn in het licht van de leeftijd en de klinische toestand van de patiënt ([14]).
Huidafwijkingen
Er zijn geen systematische reviews betreffende huidafwijkingen bij coeliakie. Dermatitis herpetiformis, een sterk jeukende, microvesiculaire uitslag op ellebogen, knieën en billen, gaat altijd gepaard met autoantilichamen tegen epidermaal transglutaminase (TG3), vergelijkbaar met TG2 (weefseltransglutaminase). Andere overeenkomsten met coeliakie zijn de relatie met HLA-DQ2 en -DQ8 en de relatie met gluten. Er bestaat vaak een enteropathie, soms beperkt tot infiltratie van lymfocyten; 15% van de patiënten heeft daarmee samenhangende klachten. Bijna altijd is de coeliakieserologie positief ([63]).
Diabetes mellitus type 1 (DM1) en andere auto-immuunziekten
In een gestructureerde review lieten De Graaff et al. zien dat bij 1,5 tot 10% van de DM1-patiënten positieve coeliakieserologie wordt gevonden, kennelijk onafhankelijk van leeftijd, ras, of ziekteduur ([31]). Positieve serologie gaat in 44-100% gepaard met histologisch bewezen coeliakie. Deze bevindingen komen overeen met die van een klinische review van Barker ([11]). Voor andere auto-immuunziekten is het beeld minder helder. Systematische reviews ontbreken en uit het gepubliceerde materiaal komt geen noodzaak naar voren om coeliakiescreening in te zetten in geval van bijvoorbeeld schildklieraandoeningen of alopecia ([112]).
Syndroom van Down, Turner en Williams
Er zijn geen systematische reviews gepubliceerd over de prevalentie van coeliakie bij Downsyndroom, maar algemeen worden percentages rond 5-7% aangehouden ([108]). In alle richtlijnen voor downsyndroom en coeliakie wordt coeliakiescreening aangeraden. Ook bij het syndroom van Turner wordt screening aangeraden vanwege verhoogde incidentie, maar net als bij het syndroom van Williams ontbreken systematische reviews ([48]).
Eerstegraadsfamilieleden
Coeliakie heeft met HLA-DQ2 en -DQ8 een sterke erfelijke basis en het is dan ook niet verwonderlijk dat het risico van coeliakie bij eerstegraadsfamilieleden verhoogd is. Het risico varieert met de wijze van overerving van het HLA-complex tussen < 1 en 28% en bedraagt gemiddeld 10,1% ([17]). Alle richtlijnen raden aan om (in elk geval de minderjarige) eerstegraadsfamilieleden van coeliakiepatiënten te screenen. Systematisch onderzoek naar de effecten van screening is niet uitgevoerd.
Tabel 9.3.1. Symptomen van coeliakie (ESPGHAN-richtlijn) ([60])
| Symptoom | Kinderen* | Alle patiënten* |
| Anorexie | 26-35 | 8 |
| Braken | 26-33 | |
| Buikpijn | 11-90 | 8-12 |
| Opgezette buik | 28-39 | 10 |
| Flatulentie | 5 | |
| Diarree | 12-75 | 13-51 |
| Onregelmatige defecatie | 4-12 | |
| Obstipatie | 4-12 | |
| Gewichtsverlies | 6-60 | |
| Groeiachterstand | 20-31 | 19 |
| ‘Niet gedijen’ | 48-89 | |
| Prikkelbaarheid | 10-14 | |
| Chronische vermoeidheid | 7 | |
| IJzergebreksanemie | 3-16 | |
| Overige vormen van anemie | 3-23 | |
| Hypertransaminasemie | 5 |
*Prevalentie (%) waarmee deze bevindingen voorkomt bij coeliakie volgens de literatuur.
Tabel 9.3.2. Associaties met coeliakie (ESPGHAN-richtlijn) ([60])
| Aandoening | Kinderen* | Alle patiënten* |
| Juveniele idiopathische artritis | 1.5-2.5 | |
| Downsyndroom | 5.5 | 0.3 |
| Turnersyndroom | 6.5 | |
| Williamssyndroom | 9.5 | |
| IgA-nefropathie | 4 | |
| IgA-deficiëntie | 3 | |
| Auto-immuunschildklierziekte | 3 | |
| Auto-immuunleverziekte | 13.5 |
*Prevalentie (%) waarmee deze bevindingen voorkomt bij coeliakie volgens de literatuur.
Tabel 9.3.3. Niet-gastro-intestinale manifestaties van coeliakie (NASPGHAN-richtlijn) ([58])
| Sterk tot matig bewijs |
|
| Minder sterk bewijs |
|
Tabel 9.3.4. Geassocieerde aandoeningen (NASPGHAN-richtlijn) ([58])
|
|
|
|
|
|
|
In de richtlijn voor volwassenen van het American Gastroenterological Association (AGA) Institute wordt volstaan met de opmerking dat ‘testing for celiac disease should be considered in symptomatic individuals who are at particularly high risk.’ Deze hoogrisicogroepen zijn gelijk aan die welke door de hierboven aangehaalde richtlijnen worden gehanteerd. De toevoeging ‘symptomatische personen’ wijkt af van de bovengenoemde adviezen, die echter specifiek op kinderen zijn gericht (Anonymous, 2006).
Conclusie:
zie Signaleren van Coeliakie,
3.3 Lactose-intolerantie
Symptomen
Lactose-intolerantie uit zich in maag-darmklachten als opgeblazen gevoel, flatulentie en buikpijn, en in ernstiger gevallen diarree, niet in afwijkingen bij lichamelijk onderzoek.. Zie Signaleren.
Preventie van lactose-intolerantie: technieken.
Preventie van klachten door lactose-inname kan in essentie op twee manieren worden bereikt: door vermindering van blootstelling aan lactose in de dunne darm (lactosebeperking in de voeding) en door optimalisering van de fermentatie van overtollig lactose in de dikke darm ([139]).
Bacteriën kunnen op twee manieren een rol spelen bij deze preventie: de lactoseconcentratie in yoghurt is lager dan in melk door de aanwezigheid van bètagalactosidaseproducerende bacteriën, en probiotica lijken, onafhankelijk van de bètagalactosidaseactiviteit, gasvorming en diarree te kunnen verminderen door hun invloed op de colonbacteriën ([34]).
Zie Preventie: effect van interventies
Aanbevelingen
3.3.1 Signaleren van lactose-intolerantie
Symptomen en afwijkingen bij lichamelijk onderzoek.
Lactosemalabsorptie leidt niet tot significante energie- of vochttekorten: het (geringe) overmatige verlies wordt gemakkelijk gecompenseerd. Er zijn dan ook geen studies die zich hebben gericht op fysieke afwijkingen die het gevolg zijn van of kunnen wijzen op lactose-intolerantie. Bij lactose-intolerantie staan de klinische symptomen op de voorgrond.
Conclusie
Lactose-intolerantie uit zich in maag-darmklachten als opgeblazen gevoel, flatulentie en buikpijn, en in ernstiger gevallen diarree, niet in afwijkingen bij lichamelijk onderzoek. Dit zijn echter aspecifieke klachten met zeer geringe voorspellende waarde. Lactose-intolerantie is alleen te verwachten bij personen met een hoge lactoseconsumptie (minimaal 12 g = 240 ml per dosis, 24 g = 480 ml per dag). Lactose in andere (voedings)middelen dan vloeibare zuivelproducten, zoals in pannenkoeken, tabletten en tandpasta, veroorzaakt geen intolerantie.
Onderbouwing
Jellema et al. (2010) onderzochten in een meta-analyse de betrouwbaarheid van klinische symptomen voor de diagnose lactose-intolerantie ([70]). Noch buikpijn of diarree, noch zelfrapportage van symptomen na melkingestie bleek een betrouwbare index te zijn van lactose-intolerantie. Zelfs van ‘symptomen na lactose-ingestie’ waren sensitiviteit en specificiteit onvoldoende voor een betrouwbare diagnose van lactose-intolerantie.
De meta-analyse van Savaiano et al. richtte zich op onderzoeken waarin dubbelblinde tests waren verricht bij personen met bewezen lactosemalabsorptie, bij wie provocatie (lactoseconsumptie) werd vergeleken met placebo ([114]). Voor flatulentie, opgeblazen gevoel, buikpijn en defecatiefrequentie werden geen significantie verschillen gevonden. Alleen voor diarree werd een significant, maar zeer klein verschil in incidentie gevonden van 0,15 (95%-betrouwbaarheidsinterval 0,03-0,28). De auteurs concludeerden dat lactosegebruik geen relevante oorzaak was van symptomen bij normale lactoseconsumptie.
Verder zijn er twee Amerikaanse consensus statements verschenen: een voor de NIH en een zeer uitgebreide en diepgaande voor het Department of Health and Human Services (DHHS) ([20]; [139]). Beide concentreren zich op de consequenties van lactose-intolerantie voor voeding en gezondheid en volstaan met een korte beschrijving van de bijbehorende klachten: opgeblazen gevoel, flatulentie, buikpijn, diarree. Het DHHS-rapport geeft bovendien een uitstekende (narratieve) analyse van de factoren die de kans op klachten (intolerantie) bij personen met hypolactasie bevorderen, zoals de aanwezigheid van het prikkelbaredarmsyndroom ([139]).
Dieetgegevens
Lactose-intolerantie is een zich tot het maag-darmstelsel beperkend probleem dat pas optreedt als de lactose-inname zowel de absorptiecapaciteit van de darm als de ‘salvage’-capaciteit van de koolhydraatfermenterende bacteriën in het colon overschrijdt ([139]). Aangezien matige hoeveelheden lactose (tot 12 g per portie en tot 24 g verspreid over de dag) bij lactose-intolerante personen goed worden verdragen, kan lactose-intolerantie als oorzaak van gastro-intestinale klachten al op voorhand worden uitgesloten als de lactose-inname beneden deze waarden blijft ([139]).
Leeftijd
Hypolactasie is een leeftijdsgebonden fenomeen. De incidentie van lactose-intolerantie is bij jonge kinderen van alle rassen zeer laag en blijft bij blanken laag tot op volwassen leeftijd, terwijl bij andere rassen de incidentie toeneemt op schoolleeftijd ([139]). Bij jonge kinderen met maag-darmklachten hoeft dus niet aan lactose-intolerantie te worden gedacht.
3.3.2 Diagnostiek
Beschouwing over de diagnostiek
Naast specifieke tests als genetisch onderzoek, lactasebepaling in het darmslijmvlies en de lactose-waterstofademtest (die alle alleen geschikt zijn om lactasedeficiëntie vast te stellen, niet voor lactose-intolerantie) is de enige betrouwbare manier om lactose-intolerantie vast te stellen eliminatie van lactose uit de voeding en herintroductie ervan. De uitkomst wordt echter vaak sterk gekleurd door de verwachtingen van de patiënt. Dubbelblinde tests vallen meestal negatief uit ([45]). Het is dus aannemelijk dat de diagnose lactose-intolerantie in de praktijk te vaak wordt gesteld (en dat de voorgeschreven dieetmaatregelen daarbij bovendien te streng zijn).
3.3.3 Preventie: effect van interventies
Conclusie
Lactosebeperking is alleen zinvol voor die personen met hypolactasie bij wie niet alleen sprake is van lactosemalabsorptie, maar ook van lactose-intolerantie. Deze situatie is bij kinderen zeldzaam. Beperking van het lactoseaanbod tot 12 g per portie en 24 g per dag (d.w.z. tot respectievelijk 240 en 480 ml melk; voor andere producten, yoghurt in de eerste plaats, gelden grotere hoeveelheden) leidt bij vrijwel alle individuen met lactose-intolerantie tot verdwijnen van de daardoor veroorzaakte gastro-intestinale klachten. Andere maatregelen, zoals probiotica, hebben geen bewezen effectiviteit.
Ervan uitgaande dat bij beperking van de lactose-inname wordt gezorgd voor adequate vervanging en dus voor een volwaardige voeding, zijn de nadelige gevolgen ervan beperkt. Er is bewijs van matige kwaliteit dat lactosereductie leidt tot verminderde botmineralisatie en verhoogd fractuurrisico. Er is verder enig bewijs dat zuivelgebruik gecorreleerd is met darmkanker.
Onderbouwing
Positieve effecten
De studie van Wilt et al. betreft een zeer uitgebreide meta-analyse van publicaties op het gebied van lactose-intolerantie en gezondheid, uitgevoerd voor het Amerikaanse Department of Health and Human Services ([139]). Hieruit kwam naar voren dat eenmalige doses tot 12 g en een dagelijkse consumptie tot 24 g lactose over het algemeen goed worden verdragen. Hogere doses veroorzaken bij meer personen klachten: een eenmalige dosis van 50 g gaf vrijwel altijd klachten ([139]). De kans dat lactose in de voeding klachten veroorzaakt, kan worden verkleind door spreiding over de dag, consumptie van melk tijdens de maaltijden en door gewone melk te vervangen door yoghurt. Voor deze laatste maatregel werd in de genoemde meta-analyse echter onvoldoende wetenschappelijke onderbouwing gevonden ([139]).
Ook Shaukat et al. komen in een systematische review tot de conclusie dat matige lactosebeperking (tot maximaal 12-15 g lactose per consumptie) over het algemeen goed wordt verdragen ([118]). Zij vonden onvoldoende bewijs voor de stelling dat melk met een verlaagd lactosegehalte minder maag-darmklachten gaf dan gewone melk. Ook voor andere behandelopties, zoals toediening van probiotica en geleidelijke verhoging van het lactoseaanbod, werd onvoldoende bewijs van effectiviteit gevonden ([118]).
Negatieve effecten
Maag-darmklachten. In de meta-analyse van Wilt et al. is alle beschikbare informatie verzameld aangaande de effecten van lactosebeperking op de gezondheid ([139]). Zij concluderen dat er geen directe informatie beschikbaar is over nadelige langetermijneffecten op de gastro-intestinale gezondheid. De consistente rapportage van lager melkgebruik door personen met hypolactasie dan door personen met lactasepersistentie suggereert dat deze strategie wordt gevolgd omdat ze leidt tot minder door zuivel veroorzaakte maag-darmklachten ([139]).
Botmineralisatie. Wilt et al. laten zien dat verminderde lactose-inname directe consequenties heeft voor de calciuminname bij zowel kinderen als volwassen veganisten ([139]). Het onderzoek naar effecten van verminderde lactose-inname op de botkwaliteit is relatief schaars en van lage kwaliteit. Er is bewijs van lage kwaliteit dat verminderde melkinname onafhankelijk is geassocieerd met slechtere botmineralisatie en verhoogde kans op fracturen; dit geldt voor prepubertaire kinderen en oudere vrouwen, niet voor volwassen mannen ([139]).
Darmkanker. Szilagyi et al. evalueerden studies naar het effect van zuivelgebruik op het risico van darmkanker ([128]). Zij vonden dat laag zuivelgebruik een beschermend effect had tegen colorectaal carcinoom, maar alleen in populaties met een hoog (> 80%) of laag (< 20%) percentage personen met hypolactasie (risicoreductie 16-20%). In gemengde populaties was dat effect echter niet aantoonbaar ([128]). Er was geen relatie met het ontstaan van darmpoliepen. Wilt et al. rapporteren niet over de relatie tussen lactose-intolerantie en kanker, hoewel de combinatie wel in hun zoekstrategie was opgenomen ([139]).
Andere effecten.
Een van de aanbevelingen van Wilt et al. is dat nader onderzoek wordt gedaan naar de effecten van lactosebeperking op aandoeningen als obesitas, diabetes mellitus, cardiovasculaire aandoeningen en kanker ([139]). Een aanvullende zoekstrategie gericht op deze combinaties leverde inderdaad geen artikelen op.
3.4 Voedseladditieven
Effecten van Voedseladditieven
De meta-analyse en RCT’s zijn samengevat in tabel 12.3.1. Twee RCT’s van goede kwaliteit (Jadad-score 5, zie 1.5 Wetenschappelijke onderbouwing) met grote aantallen gezonde kinderen evenals een recent Nederlands gerandomiseerd onderzoek bij kinderen met ADHD worden hieronder uitgebreider besproken ([12]; [83]; [100]). De meta-analyse is gericht op onderzoek naar het effect van kunstmatige kleurstoffen op het gedrag van kinderen met en zonder ADHD ([115]). 5 van de 11 AMSTAR-criteria (zie 9.4 Wetenschappelijke onderbouwing) voor het beoordelen van de kwaliteit van een SR konden niet beantwoord of moesten negatief beantwoord worden. In deze studie zijn 15 dubbelblinde placebogecontroleerde onderzoeken meegenomen van matige kwaliteit. Samen bevatten deze 15 studies 219 deelnemers met ADHD. De meeste studies betroffen slechts een klein aantal (n < 20-30) geselecteerde kinderen. Uit de meta-analyse blijkt dat kunstmatige kleurstoffen hyperactiviteit bij deze kinderen bevorderen. Het effect van de kleurstoffen gemeten met verschillende hyperactiviteittesten is 0,28 (95% BI 0,08-0,49) SD (standaarddeviatie). Ervan uitgaande dat kinderen met ADHD in hyperactiviteittesten + 2 SD’s hoger scoren dan normale kinderen is het effect van voedseladditieven bij een individueel kind niet indrukwekkend. Daarnaast werd een tweede analyse uitgevoerd, waarbij alleen gezonde kinderen zonder ADHD werden betrokken. Deze analyse had betrekking op 132 kinderen uit 7 studies van matige kwaliteit. Het betrof hier wederom studies met een klein aantal (n < 20-30) kinderen. Er werd geen statistisch significant effect van kunstmatige kleurstoffen op het gedrag van deze gezonde kinderen gevonden. De conclusie van de SR is dat kunstmatige kleurstoffen het gedrag van een deel van de kinderen met ADHD negatief kan beïnvloeden ([115]).
Tabel 12.3.1 Samenvatting van de meta-analyse en RCT’s van voedseladditieven bij kinderen met en zonder ADHD
| auteur jaar | n | leeftijd jaar | ADHD | voedseladditief | uitkomstmaat | effect | kwaliteit onderzoek |
| Schab 2004* (Schab en Trinh, 2004) | 219 (15 studies) | < 18 | ja | verschillende synthetische kleurstoffen | meestal Conners-test | ja: 0,28 SD (95% BI 0,08- 0,49) | matig (AMSTAR-score) |
| Schab 2004* (Schab en Trinh, 2004) | 132 (7 studies) | < 18 | nee | verschillende synthetische kleurstoffen | meestal Conners-test | nee | matig (AMSTAR-score) |
| Egger 1985 (Egger et al., 1985) | 28 | 2-15 | ja | melk, sinaasappelsap, tarwe, E102 of benzoëzuur | Conners-test, Porteus Maze-test | nee | matig door klein aantal geselecteerde kinderen |
| Carter 1993 (Carter et al., 1993) | 19 | 2-12 | ja | kleurstoffen: E102, E104, E110, E122, E123, E124, E127, E127 en/of sinaasappelsap, appelsap, chocolade | meerdere testen, o.a. Conners-test | ja | matig door klein aantal geselecteerde kinderen |
| Dengate 2002 (Dengate en Ruben, 2002) | 27 | 4-12 | ja | calciumpropionaat ((brood) conserveermiddel) | Rowe Behaviour Rating Inventory | nee | matig door klein aantal geselecteerde kinderen |
| Bateman 2004 (Bateman et al., 2004) | 277 | 3 jaar | nee | kleurstoffen: E102, E110, E122, E124 en natriumbenzoaat | Weiss-Werry-Peters-test | onderzoekers nee, ouders ja | goed (Jadad-score) |
| McCann Lancet 2007 (McCann et al., 2007) | 297 | 3 en 8/9- jaar | nee | kleurstoffen E102, E104, E110, E122, E124, E129 en natriumbenzoaat | ADHD-IV test, Weiss-Werry-Peters-test, observatie in de klas, Conners-test | ja, (0,12- 0,20 SD) onafhankelijk van pre-existente hyperactiviteit | goed (Jadad-score |
* meta-analyse. E102 tartrazine (citroengeel); E104 chinolinegeel; E110 oranjegeel; E122 karmozijn (rood); E123 amarant (paarsrood); E124 ponceau (rood); E127 erythrosine (rood); E133 briljantblauw; E142 groen S; E211 natriumbenzoaat, conserveringsmiddel; Conners-test: test voor oppositionele, cognitieve problemen, verminderde attentiespanne, hyperactiviteit, angstig, perfectionisme, sociale problemen, psychosomatiek, DSM-IV-symptomen; Porteus Maze-test: non-verbale intelligentietest; Rowe Behaviour Rating Inventory: test prikkelbaarheid, onrust, verstoring van de slaap; Weiss-Perry-Peters-test: hyperactiviteittest.
Bateman onderzocht in een dubbelblinde, placebogecontroleerde cross-overstudie van goede kwaliteit de invloed van kunstmatige kleurstoffen en benzoaten in de voeding bij 397 gezonde kinderen van ca. 3 jaar oud ([12]). De kinderen kregen een dieet waarbij in week 1 kleurstoffen en benzoaten werden geëlimineerd. In de 3 weken hierna kregen zij kleurstoffen en benzoaat of placebo gesuppleerd. De kinderen vertoonden meer hyperactief gedrag tijdens de periode met voedseladditieven vergeleken dan tijdens de placeboperiode. Het resultaat was onafhankelijk van pre-existente hyperactiviteit van het kind ([12]). Dit resultaat werd echter alleen door ouders waargenomen en was niet aantoonbaar door de onderzoekers. 30% van de kinderen (in beide armen van de studie) stopte voor het einde van het onderzoek.
McCann heeft eveneens een gerandomiseerde placebogecontroleerde cross-overstudie verricht bij 3- en 8/9-jarigen waarbij het effect van verschillende synthetische kleurstoffen en natriumbenzoaat onderzocht werd ([83]). Het onderzoek van goede kwaliteit betreft een groot aantal gezonde kinderen die niet voorgeselecteerd waren op hyperactiviteit of ADHD: 153 3-jarigen en 144 8/9-jarigen. 30 (10%) kinderen hebben het onderzoek niet afgemaakt. Het uitvalpercentage verschilde niet per groep. De aanwezigheid van kleurstoffen en natriumbenzoaat leidde tot meer hyperactief gedrag in beide leeftijdsgroepen. Het gemiddelde effect gemeten met verschillende testen varieerde van 0,12 SD (95% BI 0,02-0,23) tot 0,20 SD (95% BI 0,01-0,39). Als de gemiddelde hyperactiviteit van kinderen met ADHD 2 SD’s boven die van gezonde kinderen ligt, zullen voedseladditieven slechts 10% van het verschil in gedrag tussen een kind met ADHD en een kind zonder ADHD verklaren.
Recent is in een Nederlands RCT van matige kwaliteit bij een geselecteerde groep 4- tot 8-jarige kinderen met ADHD (n = 30) gekeken naar het effect van een eliminatiedieet ([100]). Alleen kinderen met ADHD die positief reageerden op een open eliminatiedieet kwamen in aanmerking voor de studie, hierdoor zijn de resultaten niet generaliseerbaar naar gezonde kinderen. Bij 19 van de 30 kinderen recidiveerden de ADHD-klachten na reïntroductie van drie voedingsmiddelen. Hoewel per individu in een cross-overopzet dubbelblind 3 lage of hoge specifieke IgG positieve voedingsmiddelen werden gegeven, waren de gevolgen op het gedrag van het kind niet op basis van de mate van IgG-positiviteit te voorspellen. In dit onderzoek werd niet gebruikgemaakt van dubbelblinde vergelijking met placebo.
Overige overwegingen
Internationale richtlijnen (over voedselallergie) geven geen advies over voedseladditieven (Engeland: NICE-guideline, Verenigde Staten: National Guideline Clearinghouse). Wel adviseert de Engelse Food Standards Agency, naar aanleiding van het in Engeland uitgevoerde onderzoek van Bateman en McCann, niet alleen ouders van kinderen met hyperactiviteit maar ook de voedselindustrie om de 6 kunstmatige kleurstoffen (E102, E104, E110, E122, E129 en E124) betrokken in het onderzoek, te vermijden ([145]; [12]; [115]). In de Europese Unie moet sinds juli 2010 op voedseletiketten niet alleen staan welke kunstmatige kleurstoffen gebruikt zijn, maar ook de waarschuwing dat deze stoffen een negatief effect op activiteit en aandacht van kinderen kunnen hebben. De waarschuwing luidt: ‘Azo-kleurstoffen kunnen een allergische reactie uitlokken en hyperreactiviteit veroorzaken bij kinderen’ ([147]).
Er is weinig gerandomiseerd onderzoek naar het effect van voedseladditieven op het gedrag van gezonde kinderen. De meeste onderzoeken naar het effect van synthetische kleurstoffen en conserveringsmiddelen richten zich op kinderen met ADHD. Mogelijk zouden voedseladditieven bij deze kinderen wel een negatief effect kunnen hebben. Daarbij speelt mee dat het ene kind met ADHD mogelijk gevoeliger is voor bepaalde stoffen dan het andere kind. Maar ook bij deze groep kinderen is er nog niet voldoende bewijs om te stellen dat zij voedseladditieven moeten vermijden, daar het weliswaar dubbelblind placebogecontroleerde onderzoeken betreft, maar steeds bij kleine aantallen geselecteerde kinderen. In een recent rapport komt het RIVM tot dezelfde conclusies en suggereert dat aanvullend onderzoek is nodig is ([152]; [168]).
Suiker
Sommige ouders zijn ervan overtuigd dat hun kind na het eten van suiker hyperactief wordt. In de pers wordt hier ook regelmatig aandacht aan besteed. De hypothese dat suiker het gedrag van kinderen negatief beïnvloedt wordt echter niet bevestigd door wetenschappelijk onderzoek. In een meta-analyse van Wolraich et al. werden 16 dubbelblinde placebogecontroleerde onderzoeken betrokken waarbij aan 560 kinderen met of zonder ADHD suiker of een placebo (meestal aspartaam) werd gegeven ([140]). De meta-analyse was van goede kwaliteit, maar de individuele RCT’s betroffen vaak geselecteerde (kinderen met ADHD of gezonde kinderen die volgens ouders reageren op suiker) en voor een deel kleine (n = 5-30) aantallen kinderen waarvan het merendeel jongens waren. De meta-analyse vond geen effect van suiker op het gedrag van kinderen ([140]).
Aanbevelingen
4 Begeleiden en behandelen
4.1 Behandelen van koemelkallergie
De basisbehandeling van koemelkallergie bestaat uit de eliminatie van koemelkeiwit. Kinderen die allergisch zijn voor koemelk worden behandeld met gehydrolyseerde koemelk op basis van wei-eiwit of caseïne, met kunstvoeding op basis van vrije aminozuren of met sojamelk. Veelbelovend is de behandeling met voeding op basis van rijsthydrolysaat. Omdat rijstproducten in Nederland niet commercieel verkrijgbaar zijn, worden ze hier buiten beschouwing gelaten.
Aanbevelingen
4.1.1 Effecten op groei
Groei is een belangrijke parameter bij de beoordeling van de effectiviteit van de verschillende soorten voeding. Er is weinig onderzoek verricht naar verschillen in groei op lange termijn bij gebruik van de diverse soorten kunstvoeding bij kinderen met koemelkallergie. De verschillende soorten kunstvoeding die gegeven worden bij koemelkallergie zouden in een vergelijkbare groei moeten resulteren als borstvoeding bij kinderen zonder koemelkallergie ([42]).
Bij kinderen met koemelkallergie bestaat de kans dat ze minder goed groeien in de eerste 6 levensmaanden ([42]). Dit hangt mogelijk (ten dele) samen met de voedingswaarde van de koemelkvervangende kunstvoeding ([42]). Bij hydrolysaten blijkt de groei in het eerste half jaar normaal te verlopen. Ook is de groei (lengte en gewicht) bij kinderen met koemelkallergie die gevoed worden met kunstvoeding op basis van vrije aminozuren even goed als die van kinderen die gevoed zijn met kunstvoeding op basis van caseïne ([42]; [133]).
Er is onderzoek dat uitwijst dat kunstvoeding in de periode van 6 tot 12 maanden op basis van wei-eiwit of caseïne resulteert in een grotere gewichtstoename dan sojamelk. Of dit gunstig of juist niet gunstig is, is niet duidelijk. In lengtegroei is geen verschil gevonden tussen gehydrolyseerde voeding en sojamelk ([42]). Bovendien kunnen op basis van klinische trials op de leeftijd van 48 maanden geen verschillen in voedingsstatus worden aangetoond tussen kinderen met koemelkallergie die gevoed zijn met gehydrolyseerde kunstvoeding en diegenen die gevoed zijn met sojavoeding ([42]). Andere studies geven aan dat er bij kinderen met koemelkallergie geen verschil bestaat in groei tussen kinderen die gevoed zijn met gehydrolyseerde kunstvoeding, voeding op basis van vrije aminozuren tot de leeftijd van 180 dagen en sojavoeding ([23]; [151]; [90]). Aan de andere kant hebben sommige kinderen met niet-IgE gemedieerde koemelkallergie mogelijk een betere lengtegroei met kunstvoeding op basis van vrije aminozuren dan met gehydrolyseerde voeding ([90]).
In een systematische review van ongewenste effecten van voeding op basis van soja blijkt uit dierexperimenteel onderzoek een mogelijk effect van plantaardige oestrogenen op de voortplanting. Er is geen onderzoek van het effect van sojavoeding op de voortplantingsorganen bij de mens ([84]).
4.1.2 Tolerantieontwikkeling
Het natuurlijke beloop van koemelkallergie is niet geheel duidelijk omdat de weinige studies die hiernaar verricht zijn niet uniform zijn qua opzet. Duidelijk is dat koemelkallergie vaak niet tot de volwassen leeftijd blijft bestaan.
Uit een studie in een academisch ziekenhuis in de Verenigde Staten is gebleken dat bijna alle kinderen koemelkallergie in hun eerste levensjaar hadden ontwikkeld. Ongeveer 80% heeft klinische tolerantie ontwikkeld op de 5e verjaardag. Bijna 35% van deze kinderen ontwikkelden allergieën voor andere voedingsmiddelen, dit blijkt uit zelfrapportage ([18]). Kinderen met persisterende koemelkallergie hadden tijdens de eerste 2 levensjaren een hogere IgE-waarde dan de kinderen die tolerantie ontwikkelden.
Andere voorspellende factoren voor het ontwikkelen van tolerantie zijn de afwezigheid van astma of allergische rinitis en het nooit hebben gekregen van kunstvoeding. In een selecte patiëntenpopulatie bleek ook de snelheid waarmee de IgE-waarden daalden voorspellend te zijn voor de ontwikkeling van koemelktolerantie ([18]). Kinderen met een vertraagde allergische reactie zouden sneller tolerant worden dan kinderen met een acute reactie ([42]).
Er bestaan aanwijzingen dat blootstelling aan kleine doses koemelk geassocieerd is met persisterende koemelkallergie ([42]). Aan de andere kant worden kleine hoeveelheden melk verwerkt in producten soms goed verdragen en is het bij afwezigheid van klachten niet nodig deze uit het dieet te elimineren ([72]). Kleine hoeveelheden melk verwerkt in verhitte producten (bv. koekjes) worden vaak beter verdragen dan die in niet-verhitte producten en kunnen tolerantie voor koemelk zelfs versnellen ([93]).
Terracciano et al. vonden in een gerandomiseerde studie bij een geselecteerde groep kinderen in een derdelijnscentrum dat bij behandeling met soja of aminozuren van kinderen die niet allergisch zijn voor soja de duur van de koemelkallergie korter is in vergelijking met behandeling met koemelkhydrolysaat, waarin nog een residu aanwezig is van koemelkeiwit, namelijk gemiddeld 28 versus gemiddeld 56 maanden ([129]).
Op basis van de beschikbare literatuur is het niet mogelijk een uitspraak te doen welk type voeding de voorkeur heeft ten aanzien van de snelheid van tolerantieontwikkeling voor koemelk.
Introductie van bijvoeding vanaf 4 maanden wordt ook bij kinderen met koemelkallergie aanbevolen omdat het de kans op allergie voor andere voedingsmiddelen (zoals bv. kippenei of pinda’s) of voor andere uitingen van allergie (zoals astma) niet vergroot en mogelijk zelfs verkleint.
4.1.3 Reïntroductie van koemelk
Reïntroductie vanaf 1 jaar
Er zijn enkele studies die hebben aangetoond dat verschil in tolerantie afhankelijk is van het type koemelkallergie (wel of niet IgE-gemedieerd) ([42]). Op basis hiervan beveelt de DRACMA aan om op de leeftijd van 1 jaar koemelk te reïntroduceren bij niet-IgE-gemedieerde koemelkallergie, terwijl hiermee bij IgE-gemedieerde allergie beter nog wat langer gewacht kan worden, afhankelijk van de uitslagen van herhaalde allergietesten ([42]). Uiteraard is de anamnese van groot belang: als blijkt dat niet-opzettelijke inname van een geringe hoeveelheid koemelk tot klachten heeft geleid, moet langer worden gewacht met herevaluatie van de koemelkallergie. Het wordt aanbevolen om kinderen niet langer dan noodzakelijk een eliminatiedieet te geven ([76]). Het is tot op heden niet duidelijk of onnodige eliminatie leidt tot juist het ontwikkelen van koemelkallergie in plaats van tot tolerantieontwikkeling.
Vanaf de leeftijd van 1 jaar kan elk half jaar worden bekeken of het kind nog allergisch is ([76]). Bij persisteren van koemelkallergie na de leeftijd van 1 jaar en bijkomende problematiek wordt verwezen naar de kinderarts. Bij een ongecompliceerd verloop blijft het kind in de eerste lijn. Zijn er bij reïntroductie geen klachten meer, dan kan het kind vanaf dat moment weer koemelk gebruiken. Reïntroductie van koemelk bij kinderen met een verhoogd risico op een ernstige allergische reactie dient door de kinderarts te worden begeleid. Dit betreft kinderen met luchtwegklachten/astma en eerder doorgemaakte ernstige reacties.
Vaccinaties
Alle vaccins in het Rijksvaccinatieprogramma zijn veilig voor kinderen met koemelkallergie en kippeneiallergie ([165]). Het vaccin tegen influenza zou bij sommige kinderen met ernstige kippeneiallergie een allergische reactie kunnen veroorzaken en wordt alleen in overleg met de huisarts/kinderarts gegeven ([167]). Vaccins tegen gele koorts en rabiës zijn gecontraïndiceerd bij kinderen met kippeneiallergie.
5 Totstandkoming
5.1 Werkgroep
Projectgroep
- Mw. dr. J.E. Kist-van Holthe, kinderarts en projectleider, VUmc/EMGO+ -instituut, Amsterdam
- Mw. dr. A.M.W. Bulk-Bunschoten, arts maatschappij en gezondheid, VUmc/EMGO+- instituut, Amsterdam
- Prof. dr. R.A. HiraSing, hoogleraar jeugdgezondheidszorg, VUmc/EMGO+-instituut, Amsterdam
- Mw. drs. S. Kalidien, gezondheidswetenschapper en projectmedewerker, VUmc/ EMGO+-instituut, Amsterdam
- Dr. C.M.F. Kneepkens, kinderarts maag-darm-leverziekten, VUmc, Amsterdam
- Mw. dr. M.L.A. de Kroon, jeugdarts-epidemioloog en coördinator Academische Werkplaats Noord-Holland, VUmc/EMGO+-instituut, Amsterdam
- Dr. T. Kuijpers, epidemioloog, CBO, Utrecht
- Mw. dr. A.B. Sprikkelman, kinderarts-pulmonoloog, Emma Kinderziekenhuis AMC, Amsterdam
- Mw. dr. B.J. Vlieg-Boerstra, diëtist en postdoctoraal onderzoeker, Emma Kinderziekenhuis AMC, Amsterdam, Erasmus MC, sectie Allergologie, Rotterdam, Nederlandse Vereniging van Diëtisten
- Mw. drs. C.L. Wensing-Souren, arts maatschappij en gezondheid, Artsen Jeugdgezondheidszorg Nederland
Klankbordgroep
- Mw. E. Botjes, Patiëntenvereniging Stichting VoedselAllergie, Nijkerk
- Dr. P.L.P. Brand, kinderarts-pulmonoloog, Isala Klinieken, Zwolle
- Mw. N. Broeren, diëtist ZuidZorg, Eindhoven
- Mw. drs. E. Buiting, jeugdarts en stafarts Thuiszorg Pantein en Vivent JGZ
- Mw. dr. E. George, kinderarts maag-darm-leverziekten, Nederlandse Vereniging voor Kindergeneeskunde, Utrecht
- Mw. E. Govers, diëtist Amstelring, Amsterdam
- Dr. H. de Groot, allergoloog, Reinier de Graaf Groep, Delft
- Mw. drs. H. Jeeninga, jeugdarts, Stichting Thuiszorg Midden-Gelderland
- Mw. D. Kolkman, verloskundige, Koninklijke Nederlandse Organisatie van Verloskundigen
- Mw. drs. M. Luning, huisarts en wetenschappelijk medewerker, Nederlands Huisartsen Genootschap
- Mw. G. Lucassen, manager ZuidZorg, Eindhoven
- Mw. I. Mimpen, JGZ-kinderdiëtist, Nederlandse Vereniging van Diëtisten, Houten
- Mw. I. Parlevliet, Verpleegkundigen & Verzorgenden Nederland, Utrecht
- Dr. S. Peters, Voedingscentrum, Den Haag
- Mw. drs. H. Silvius, werkgroeplid herziening NHG-standaard voedselovergevoeligheid
- Mw. drs. C. Stegeman, jeugdarts, GGD Groningen
- Mw. drs. I Tissen, jeugdarts ZuidZorg, Eindhoven
- Mw. drs. M.van der Valk, jeugdarts, GGD Zeeland
- Mw. M. Verdel, jeugdverpleegkundige, Verpleegkundigen & Verzorgenden Nederland, Utrecht
- Mw. drs. E. Vlaanderen, jeugdarts, GGD Zaanstreek-Waterland
5.2 Historie
Vanaf 1995 worden door JGZ-medewerkers adviezen gegeven voor preventie van voedselallergie op basis van de eerste landelijke standaard voor de diagnose en behandeling van voedselovergevoeligheid, Voedselallergie bij zuigelingen op het consultatiebureau [153].Doel van de standaard was uniformiteit in de adviezen te bereiken ten aanzien van het beleid rond voedselallergie (preventie, signalering, diagnostiek, begeleiding).
n 1995 verscheen de NHG-Standaard Voedselovergevoeligheid; hiermee waren de adviezen voor preventie goed afgestemd. In de daaropvolgende jaren werden in de opeenvolgende drukken van de landelijke standaard de adviezen voor preventie steeds bijgesteld op basis van de literatuur en de adviezen van internationale beroepsorganisaties [156]. De aanpassingen betroffen onder andere het benoemen van de risicogroep (voor welke groep is selectieve preventie van belang) en de inhoud van de voedingsadviezen (soort voeding en periode van gebruik, tijdstip van introductie van de bijvoeding).
Het nut van de preventieve maatregelen werd steeds onduidelijker en van afstemming van de adviezen tussen de diverse professionals is weinig sprake, hetgeen tot verwarring leidt bij ouders. Herziening en afstemming van de preventieve adviezen zijn dus van groot belang.
5.3 Werkwijze
Voor het ontwikkelen van de richtlijn is een multidisciplinaire projectgroep samengesteld, bestaande uit vertegenwoordigers van alle specialismen die met het voorkomen van voedselovergevoeligeid bij kinderen en het signaleren, indien mogelijk diagnosticeren, begeleiden en zo nodig verwijzen van kinderen met voedselovergevoeligheid in de JGZ te maken hebben. De projectgroepleden zijn door de beroepsverenigingen gemandateerd voor deelname aan de werkgroep. De projectgroepleden zijn gezamenlijk verantwoordelijk voor de integrale tekst van deze conceptrichtlijn. Daarnaast is een klankbordgroep samengesteld, bestaande uit vertegenwoordigers van in de JGZ werkzame beroepsgroepen, van belanghebbende beroepsgroepen (huisartsen, kinderartsen en diëtisten) en van de patiëntenvereniging.
Eerst is in 2011 een knelpuntenanalyse verricht om de huidige werkwijze rondom voedselovergevoeligheid in de JGZ te inventariseren. Aan de hand hiervan zijn uitgangsvragen opgesteld. Voor het beantwoorden van de uitgangsvragen is in de literatuur systematisch gezocht naar relevant onderzoek, zie de sectie Verantwoording. De hieruit voortvloeiende conclusies en aanbevelingen vormen de basis van deze richtlijn. De uitgangsvragen betreffende signaleren, diagnostiek en verwijzen van kinderen met koemelkallergie zijn overgenomen uit de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’ [166].
5.4 Implementatie
In de verschillende fasen van de richtlijnontwikkeling is rekening gehouden met de implementatie van de richtlijn en de praktische uitvoerbaarheid van de aanbevelingen. Daarbij is bij de praktijktest expliciet gelet op factoren die op de invoering van de richtlijn in de praktijk van invloed kunnen zijn.
Nadat de richtlijn Voedselovergevoeligheid is vastgesteld, is deze aangeboden aan de JGZ (AJN, V&VN en NVDA) en de betrokken beroepsgroepen (NHG, NVK, NVD). Implementatie van de richtlijn wordt door het Nederlands Centrum Jeugdgezondheid (NCJ) uitgevoerd.
Bij de proefimplementatie van de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’ van de Nederlandse Vereniging voor Kindergeneeskunde is gebleken dat de DBPGVP in de JGZ haalbaar is.
Voor een succesvolle implementatie van deze richtlijn acht de werkgroep het noodzakelijk dat adequate diagnostiek (bij voorkeur DBPGVP) als voorwaarde wordt gesteld voor vergoeding van intensief gehydrolyseerde kunstvoeding. Het is reëel om alleen de meerkosten ten opzichte van standaardkunstvoeding te vergoeden. Overleg met de zorgverzekeraars is in gang gezet.
Verder is het noodzakelijk dat het honorarium van de jeugdarts en jeugdverpleegkundige voor het uitvoeren van de DBPGVP en OVP op het consultatiebureau vergoed gaan worden.
Implementatie van de richtlijn zal plaatsvinden tezamen met de implementatie van de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’, waarbij regionaal voor de diagnostiek en behandeling van koemelkallergie de samenwerking tussen de eerste, tweede en derde lijn geïmplementeerd zal gaan worden.
5.5 Indicatoren
Proces:
- vermoeden van koemelkallergie (koemelkvrij dieet)
- indicatiestelling voor diagnostiek koemelkallergie (door arts)
Inhoud:
- DBPGVP (dubbelblinde placebogecontroleerde voedselprovocatie)
- OVP (open voedselprovocatie) thuis
- OVP (open voedselprovocatie) op het consultatie bureau
5.6 Herziening
Na 5 jaar of zo nodig eerder bepaalt het Nederlands Centrum Jeugdgezondheid (NCJ) of de richtlijn nog actueel is. Tot die tijd zijn de aan de ontwikkeling van de richtlijn deelnemende partijen verantwoordelijk voor het melden van fouten of problemen bij de uitvoering van de richtlijn. Voor het melden van nieuwe ontwikkelingen in de wetenschap of zorgpraktijk die bijstelling of herziening van de richtlijn noodzakelijk maken, zijn de verenigingen via de individuele zorgverleners verantwoordelijk. Zo nodig wordt er een nieuwe werkgroep geïnstalleerd om de richtlijn te herzien. De geldigheid van de richtlijn komt eerder te vervallen indien nieuwe ontwikkelingen daartoe aanleiding geven.
6 Verantwoording
6.1 Knelpuntanalyse
Inleiding
Voor het ontwikkelen van de richtlijn is allereerst een inventarisatie gemaakt van de knelpunten en succesfactoren van de huidige werkwijze rondom voedselovergevoeligheid in de jeugdgezondheidszorg. In maart 2011 is een vragenlijst verstuurd naar alle JGZ-organisaties. De vragen betroffen preventie, signalering, diagnostiek en begeleiden van kinderen met voedselovergevoeligheid. De belangrijkste conclusies zijn hier samengevat.
Van de 57 GGD’en en thuiszorgorganisaties hebben 27 (47%) de vragenlijst ingevuld. Hoewel in de enquête open vragen over voedselovergevoeligheid in het algemeen werden gesteld, gingen de antwoorden altijd over koemelkallergie.
Preventie
De knelpunten die het meest genoemd worden op het gebied van preventie van koemelkallergie zijn het ontbreken van eenduidig beleid, een niet-evidence-based/verouderde landelijke standaard voedselallergie [156] en het niet volgen van het protocol door JGZ-professionals.
Signaleren/diagnostiek
Het ontbreken van duidelijke richtlijnen, eenduidige advisering en duidelijke criteria voor het vermoeden van de diagnose koemelkallergie zijn de grootste knelpunten. Vaak genoemde knelpunten op het gebied van de diagnostiek zijn dat open provocatie subjectief is en ouders niet gemotiveerd zijn voor het volledige diagnostische traject. De subjectiviteit van de provocatie die veelal thuis gedaan wordt en het ontbreken van duidelijke afspraken hierover zijn de grootste knelpunten op het gebied van diagnostiek. Verder zijn jeugdartsen en huisartsen vaak onvoldoende op hoogte van de mogelijkheden en betrouwbaarheid van de diagnostiek.
Behandeling
Dieetvoeding voor kinderen met koemelkallergie wordt volledig vergoed. Dit leidt ertoe dat ouders vaak niet gemotiveerd zijn voor het diagnostische onderzoek. Dit is een van de meest genoemde knelpunten op het gebied van begeleiden en behandelen. Verder worden op dit gebied ook het ontbreken van eenduidig beleid en het ontbreken van evidence vermeld. Andere knelpunten zijn onvoldoende afstemming/geen consensus van het beleid met kinderartsen en dat recente ontwikkelingen vaak niet bekend zijn.
Verwijzen
Knelpunten die naar voren komen op het gebied van verwijzen zijn dat er geen duidelijke afspraken over verwijzen zijn en dat er niet vaak genoeg naar een diëtist verwezen wordt.
Organisatie van de zorg
In de organisatie van zorg ervaren zorgverleners de volgende knelpunten: het ontbreken van duidelijke verwijsafspraken en eenduidig beleid, onjuiste diagnose door de huisarts, subjectiviteit en weinig terugkoppeling. De meest genoemde suggestie voor organisatorische verbetering is een betere afstemming tussen de verschillende lijnen. Dit kan leiden tot verbetering in interdisciplinaire samenwerking. Het duidelijk vastleggen van afspraken zou kunnen leiden tot verbetering in de communicatie.
Ouders
De knelpunten die door ouders ervaren worden, zijn volgens de zorgverleners de verschillende adviezen van verschillende professionals, onvoldoende begeleiding en de lange procedure.
Suggesties voor een goede richtlijn
De richtlijn zou volgens de zorgverleners rekening moeten houden met de volgende punten: afstemming tussen de eerste, tweede en derde lijn, een evidence-based richtlijn met een eenduidig preventie- en diagnostisch protocol voor koemelkallergie en aandacht voor verbetering van de communicatie met ouders.
6.2 Uitgangsvragen
Voor het ontwikkelen van de richtlijn zijn onderstaande uitgangsvragen geformuleerd. Deze uitgangsvragen zijn een zo goed mogelijke weergave van de belangrijkste knelpunten bij de aanpak van voedselovergevoeligheid bij kinderen binnen de JGZ.
Koemelkallergie
Preventie van koemelkallergie
1. Wat zijn bij zuigelingen de gewenste en ongewenste effecten van universele preventie door middel van borstvoeding, hypoallergene voeding, pre- en probiotica op voedselallergie, constitutioneel eczeem, hooikoorts en astma?
2. Wat zijn bij zuigelingen met een hoog risico op allergische aandoeningen de gewenste en ongewenste effecten van selectieve preventie door middel van borstvoeding, hypoallergene voeding, pre- en probiotica op voedselallergie, constitutioneel eczeem, hooikoorts en astma?
3. Wat zijn bij koemelkallergie de gewenste en ongewenste effecten van geïndiceerde preventie (uitstellen van de eerste introductie en soort bijvoeding) op het ontstaan van andere (voedsel)allergieën (bv. ei-allergie, pinda-allergie)?
4. Wat zijn bij hoogrisicogroepen (bv. familiaire voedselallergie) de gewenste en ongewenste effecten van selectieve preventie (uitstellen van de introductie en soort bijvoeding) op voedselallergie, constitutioneel eczeem, hooikoorts en astma?
Signaleren koemelkallergie
5. Bij welke symptomen/aanwijzingen uit de (voedings)anamnese en lichamelijk onderzoek moet worden gedacht aan koemelkallergie of overgegaan worden tot diagnostiek van koemelkallergie?
Diagnostiek van koemelkallergie
6. Welke kunstvoeding (op basis van wei-eiwit, caseïne, aminozuren of soja) is het meest geschikt in de diagnostische fase?
7. Wat zijn de gewenste en ongewenste effecten van de open en de dubbelblinde placebogecontroleerde provocatietest bij de diagnostiek van koemelkallergie?
8. Waar kunnen open en dubbelblinde placebogecontroleerde provocatietesten worden uitgevoerd: in het ziekenhuis, thuis, op het consultatiebureau, in de huisartsenpraktijk?
Verwijzen bij vermoeden van koemelkallergie
9. Welke disciplines (jeugdarts, jeugdverpleegkundige, verpleegkundig specialist, diëtist, huisarts, kinderarts) zijn het meest aangewezen om kind/ouder na de diagnose voedselallergie (met name koemelkallergie) te begeleiden?
10. Wanneer is verwijzing naar de diëtist wenselijk of vereist bij de diagnostiek van koemelkallergie?
Behandelen van kinderen met koemelkallergie
11. Wat zijn de gewenste en ongewenste effecten van de behandeling van koemelkallergie met voeding op basis van wei-eiwit, caseïne, aminozuren en soja?
12. Op welke leeftijd en door wie (jeugdarts, huisarts, diëtist, kinderarts) kan bij koemelkallergie het beste reïntroductie plaatsvinden?
Coeliakie
Preventie van coeliakie
13. Wat zijn de gewenste en ongewenste effecten van universele preventie (tijdstip en wijze van introductie gluten) van coeliakie?
Signaleren van coeliakie
14. Bij welke anamnestische (dieet)gegevens, symptomen en afwijkingen bij lichamelijk onderzoek dient aan coeliakie gedacht te worden?
Lactose-intolerantie
Klinische verschijnselen en beloop
15. Wat is er bekend over lactose-intolerantie bij specifieke bevolkingsgroepen?
Signaleren van lactose-intolerantie
16. Bij welke anamnestische (voedings)gegevens, symptomen en afwijkingen bij lichamelijk onderzoek dient aan lactose-intolerantie gedacht te worden?
Voedseladditieven
17. Wat is het effect van voedseladditieven op het gedrag van kinderen?
Bij de beantwoording van de uitgangsvragen wordt rekening gehouden met de leeftijd van het kind en de sociaal-economische positie en etnische achtergrond van het gezin. Daarnaast worden bij de beantwoording de ongewenste effecten meegewogen. De resultaten worden waar mogelijk opgesplitst in korte- en langetermijneffecten.
6.3 Literatuuronderzoek
6.3.1 Koemelkallergie
Zoeken en selecteren van de literatuur Signaleren Koemelkallergie
De uitgangsvraag en de resultaten zijn overgenomen uit de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’ van de Nederlandse Vereniging voor Kindergeneeskunde ([166]). De aanbevelingen inclusief onderbouwing van het beleid van belang voor de JGZ worden hier weergegeven. Raadpleeg voor de uitgebreide versie de betreffende richtlijn. Bij het beantwoorden van de uitgangsvraag is uitgegaan van de NICE-richtlijn (National Institute for Health and Clinical Excellence [163]). In de NICE-richtlijn zijn studies meegenomen waarin gegevens uit (voedings)anamnese, klinische verschijnselen en lichamelijk onderzoek worden geëvalueerd die aanleiding moeten geven voor een nader onderzoek naar voedselallergie. Er zijn 10 studies geselecteerd en beoordeeld. Ze bleken alle van lage kwaliteit. Daarnaast zijn 6 reviews beoordeeld op risicofactoren voor het ontstaan van voedselallergie. De afzonderlijke studies zijn beoordeeld met de GRADE-methode.
Zoeken en selecteren van de literatuur Diagnostiek Koemelkallergie
Deze uitgangsvragen zijn overgenomen uit de richtlijn ‘Diagnostiek van Koemelkallergie bij Kinderen in Nederland’ van de Nederlandse Vereniging voor Kindergeneeskunde ([166]). Aanbevelingen en onderbouwing van het beleid van belang voor de JGZ worden hier weergegeven. Bij het beantwoorden van de uitgangsvragen is uitgegaan van de DRACMA-richtlijn ([42]). Zie paragraaf 4.2.
Zoeken en selecteren van de literatuur Preventie Koemelkallergie
In eerste instantie is een zoekactie verricht naar internationale richtlijnen en systematische reviews. Deze zoekactie leverde een bruikbare (waarin uitgangsvragen over preventie waren opgenomen) en recente richtlijn op ontwikkeld in de Verenigde Staten door het National Institute of Allergy and Infectious Diseases (NIAID). Voor deze richtlijn werd een uitvoerige systematische review (van goede kwaliteit) uitgevoerd [151]. Een beknoptere versie van dit rapport werd gepubliceerd in de JAMA [29]. De beantwoording van de uitgangsvragen met betrekking tot preventie van voedselallergie is gebaseerd op deze systematische review.
De zoekactie van Chafen et al. werd verricht in september 2009. Er is op basis van de gehanteerde zoekstrategie in deze review een update van de literatuur uitgevoerd in MEDLINE t/m april 2011 naar RCT’s. Hierbij werden 49 RCT’s gevonden waarvan er uiteindelijk een aan de selectiecriteria voldeed [137].
Bij de resultaten wordt kort de systematische review van Chafen [151] samengevat, aangevuld met een samenvatting van de artikelen gevonden met de update van de literatuur. Door het ontbreken van een beschrijving van de effecten van prebiotica in de review van Chafen werd hiervoor gebruikgemaakt van twee andere reviews [98]; [131]. Bij het selecteren van de literatuur zijn de selectiecriteria in tabel 3.2.1 gebruikt.
Tabel 3.2.1 Selectiecriteria
|
Type studies |
|
|
Type deelnemers |
|
|
Type interventies |
|
|
Type uitkomsten |
|
Beschrijving studies
In de studie van Chafen (van goede kwaliteit) werden 6 systematische reviews en 47 RCT’s gevonden waarin de preventie van allergische aandoeningen werd bestudeerd [151]. 20 van de ingesloten RCT’s werden beschreven in een of meer van de systematische reviews en werden niet afzonderlijk geanalyseerd. 2 studies werden geëxcludeerd vanwege het ontbreken van data over de vergelijking tussen de interventie en de controlegroep.
Populatie
Over het algemeen bestond de populatie van de gevonden studies in de review van Chafen uit zwangere vrouwen, zuigelingen of beiden met een allergische ziektegeschiedenis [151].
Interventies
In de studies die werden ingesloten werden de volgende vijf preventiestrategieën geëvalueerd:
- dieet van de moeder gedurende de zwangerschap of lactatie (3 studies: [54]; [157]; [120]😉
- exclusieve borstvoeding (3 studies: [41]; [81]; [116]😉
- borstvoeding en het uitstellen van de introductie van de eerste bijvoeding (2 studies: [53]; [71]😉
- speciale diëten voor zuigelingen en jonge kinderen (12 studies: [7]; [10]; [33]; [32]; [55]; [82]; [95]; [96]; [97]; [126]; [136]; [135]😉
- probiotica (5 studies: [4]; [61]; [77]; [78]; [107].)
Uitkomstmaten
Cumulatieve prevalentie van allergische aandoeningen.
‘Risk of bias assessment’
De studies varieerden in kwaliteit van laag tot goed.
Zoeken en selecteren van literatuur Behandelen Koemelkallergie
Bij het beantwoorden van de eerste vraag gelden dezelfde uitgangspunten en overwegingen als bij de voeding tijdens diagnostiek van koemelkallergie. Dat betekent dat de kunstvoeding die gebruikt wordt bij diagnostiek van koemelkallergie tevens gebruikt wordt voor de behandeling. Daarnaast is van belang dat er bij de behandeling gelet wordt op gevolgen voor de groei en op de snelheid van tolerantieontwikkeling. Bij de beschrijving van de groei is gebruikgemaakt van de secties 11 (The natural history of CMA) en 14 (Guidelines for choosing a replacement formula) uit de DRACMA en voor tolerantieontwikkeling tevens van de NIAID, sectie 3.1.2 (Natural history of milk allergy) ([22]; [42]). De DRACMA heeft de literatuur in de betreffende secties niet met de GRADE-methode beoordeeld, de NIAID heeft dit met de betreffende sectie wel gedaan ([42]; [19]). Voor een update van de literatuur van juli 2008 tot maart 2011 is gebruikgemaakt van de literatuursearch van diagnostiek van koemelkallergie (n = 221), omdat bij deze search diagnostiek, behandeling, groei- en tolerantieontwikkeling niet uitgesloten zijn. Geselecteerd zijn die artikelen die zich richten op groei, tolerantieontwikkeling en/of introductie van koemelk bij kinderen met koemelkallergie: een systematische review van Chafen et al. ([29]) van goede kwaliteit, twee RCT’s, van Burks et al. en Niggeman et al. ([23]; [90]) van lage kwaliteit en een gerandomiseerd onderzoek van Terraciano et al. van voldoende kwaliteit ([129]).
6.3.2 Coeliakie
Zoeken en selecteren van de literatuur Preventie Coeliakie
In eerste instantie is een zoekactie verricht naar internationale richtlijnen en systematische reviews vanaf 2000 in MEDLINE, waarbij 14 abstracts werden gevonden. De zoekactie leverde geen bruikbare richtlijnen op (waarin uitgangsvragen over preventie van coeliakie waren opgenomen). Er werd één bruikbare systematische review ([6]) gevonden. Daarnaast werd een zoekactie uitgevoerd naar observationele studies vanaf 2000 in MEDLINE. Er werden 35 abstracts gevonden, hierbij werden geen relevante studies geselecteerd (aanvullend op de review van Akobeng). Verder werden door de werkgroep nog een viertal studies aangedragen ([51]; [59]; [91]; [164]; [121]) die worden gebruikt bij het formuleren van overige overwegingen. Deze studies hebben het karakter van narratieve reviews/theoretische beschouwingen.
Hieronder wordt de systematische review en meta-analyse van Akobeng beschreven waarin het effect van borstvoeding op het ontstaan van coeliakie werd onderzocht ([6]). In deze review werden 6 patiëntcontroleonderzoeken gevonden ([8]; [9]; [39]; [49]; [65]; [103]) waarin het risico op coeliakie werd vergeleken tussen kinderen die borstvoeding kregen en kinderen die dit niet kregen of waarin groepen met een verschillende duur van borstvoeding met elkaar werden vergeleken. De controlegroep was veelal afkomstig uit nationale registers of uit dezelfde regio. De expositie (borstvoeding) werd gemeten met een vragenlijst of een interview. Er werd gecontroleerd voor verschillende confounders (waaronder leeftijd van het kind) maar dit varieerde sterk per studie.
‘Risk of bias assesment’
De studies kregen alle het oordeel ‘matig risico op vertekening’.
Zoeken en selecteren van de literatuur Signaleren Coeliakie
In PubMed is gezocht naar meta-analyses en systematische reviews gericht op de symptomatologie van coeliakie. Dit leverde twee recente richtlijnen op voor kinderen, twee voor volwassenen, acht artikelen gericht op specifieke symptomen (vier betreffende functionele buikklachten bij volwassenen, twee over neurologische en twee over orale pathologie) en één artikel gericht op laboratoriumafwijkingen (hypertransaminasemie). Daarnaast werd gebruikgemaakt van de NICE-richtlijn ([162]) en de CBO-richtlijn Coeliakie en Dermatitis Herpetiformis ([150]).
6.3.3 Lactose-intolerantie
Zoeken en selecteren van de literatuur Preventie Lactose-intolerantie
In PubMed is gezocht naar meta-analyses en systematische reviews over preventie bij lactose-intolerantie. Dit leverde 9 artikelen op, waarvan 3 relevant voor de vraagstelling.
Zoeken en selecteren van de literatuur Signaleren Lactose-intolerantie
In PubMed is gezocht naar meta-analyses en systematische reviews gericht op de symptomatologie van lactose-intolerantie. Dit leverde vier artikelen op, die hieronder worden besproken. Deze reviews beperken zich grotendeels tot volwassenen.
6.3.4 Voedseladditieven
Zoeken en selecteren van de literatuur Voedseladditieven
Er is systematisch naar literatuur gezocht in PubMed. De volgende zoektermen zijn gebruikt: child, allergy, food additive, artificial food coloring, (Feingold) diet, behaviour and hyperactivity. Er is in eerste instantie gezocht naar systematische reviews (SR) en meta-analyses en vervolgens naar randomized controlled trials (RCT’s). Er zijn 370 artikelen gevonden, waaronder één kwalitatief redelijk goede meta-analyse over het effect van synthetische kleurstoffen uit 2004 ([115]). Na screening van de abstracts op SR’s en RCT’s bij kinderen < 18 jaar bleven er 6 RCT’s over. Eén RCT bestudeerde een conserveermiddel, twee RCT’s zijn niet gebruikt in de meta-analyse en drie RCT’s zijn gepubliceerd na het verschijnen van de meta-analyse. Daarnaast is in verschillende internationale richtlijnen gezocht naar aanbevelingen met betrekking tot intolerantie voor voedseladditieven bij kinderen.
6.4 Wetenschappelijke onderbouwing
De richtlijn is (voor zover mogelijk) gebaseerd op bewijs uit wetenschappelijk onderzoek.
Er is gestart met zoeken naar systematische reviews en richtlijnen (Cochrane Library, National Guideline Clearinghouse, National Institute for Health and Clinical Excellence (NICE)). Daarna is aanvullend systematisch gezocht naar literatuur in MEDLINE, Embase en PsycINFO tot 1 april 2011.
Systematische reviews werden beoordeeld op kwaliteit met behulp van de AMSTAR-criteria [119]. De RCT’s werden beoordeeld met de Jadad-criterialijst [66]; deze meet de methodologische kwaliteit van een studie op een schaal van 0-5, waarbij punten worden toegekend voor randomisatie, blindering, uitval en drop-outs. De kwaliteit van studies werd beoordeeld als ‘goed’ als er sprake was van een adequate randomisatie en blindering, een ‘intention to treat analyse’ werd uitgevoerd en er sprake was van een follow-uppercentage van boven de 50%. De kwaliteit van studies waarbij twee of meer van bovenstaande kenmerken niet in orde waren werd beoordeeld als ‘redelijk’, de kwaliteit van studies met minder dan twee van bovenstaande kenmerken werd beoordeeld als ‘laag’.
De literatuur is samengevat en vervolgens is een conclusie geformuleerd waarbij de kwaliteit van het bewijs is aangegeven. De kwaliteit van het bewijs werd beoordeeld met behulp van GRADE [117]. GRADE is een methode die per uitkomstmaat een gradering aan de kwaliteit van het bewijs toekent op basis van vertrouwen in de schatting van het effect op basis van de indeling in tabel 9.4.1 en 9.4.2.
Tabel 9.4.1 Indeling van de kwaliteit van het bewijs volgens GRADE
| hoog | Er is veel vertrouwen dat het werkelijke effect dicht in de buurt ligt van de schatting van het effect. |
| matig | Er is matig vertrouwen in de schatting van het effect: het werkelijke effect ligt waarschijnlijk dicht bij de schatting van het effect, maar er is een mogelijkheid dat het hier substantieel van afwijkt. |
| laag | Er is beperkt vertrouwen in de schatting van het effect: het werkelijke effect kan substantieel verschillend zijn van de schatting van het effect. |
| zeer laag | Er is weinig vertrouwen in de schatting van het effect: het werkelijke effect wijkt waarschijnlijk substantieel af van de schatting van het effect. |
Tabel 9.4.2 De kwaliteit van het bewijs wordt bepaald op basis van de volgende criteria
| Type bewijs |
RCT start in de categorie ‘hoog’. Observationele studie start in de categorie ‘laag’. Alle overige studietypen starten in de categorie ‘zeer laag’. |
||
| ‘Downgraden’ | ‘Risk of bias’ | -1 | Serieus |
| -2 | Zeer serieus | ||
| Inconsistentie | -1 | Serieus | |
| -2 | Zeer serieus | ||
| Indirectheid | -1 | Serieus | |
| -2 | Zeer serieus | ||
| Imprecisie | -1 | Serieus | |
| -2 | Zeer serieus | ||
| Publicatiebias | -1 | Waarschijnlijk | |
| -2 | Zeer waarschijnlijk | ||
| ‘Upgraden’ | Groot effect | +1 | Groot |
| +2 | Zeer groot | ||
| Dosis response relatie | +1 | Bewijs voor gradiënt | |
| Alle plausibele confounding | +1 | Zou een effect kunnen reduceren | |
| +1 | Zou een tegengesteld effect kunnen suggereren terwijl de resultaten geen effect laten zien | ||
Voor het formuleren van een aanbeveling zijn naast het wetenschappelijke bewijs vaak nog andere aspecten van belang, bijvoorbeeld: patiëntenvoorkeuren, kosten, beschikbaarheid van voorzieningen of organisatorische aspecten. Deze aspecten worden, voor zover niet wetenschappelijk onderzocht, vermeld onder ‘overige overwegingen’. In de overige overwegingen spelen dus de ervaring en de mening van de werkgroepleden een belangrijke rol. De ‘aanbeveling’ is het resultaat van de integratie van het beschikbare bewijs met de weergegeven overige overwegingen.
6.5 Kennislacunes
Aanbevelingen
Referenties
[1] American Academy of Pediatrics. Committee on Nutrition. Hypoallergenic infant formulas. Pediatrics 2000;106(2 Pt 1):346-9
https://pubmed.ncbi.nlm.nih.gov/10920165[2] . AGA Institute Medical Position Statement on the Diagnosis and Management of Celiac Disease. Gastroenterology 2006;131(6):1977-80
https://pubmed.ncbi.nlm.nih.gov/17087935[3] Aardoom HA, Hirasing RA, Rona RJ, Sanavro FL, van den Heuvel EW, Leeuwenburg J. Food intolerance (food hypersensitivity) and chronic complaints in children: the parents' perception. European journal of pediatrics 1997;156(2):110-2
https://pubmed.ncbi.nlm.nih.gov/9039513[4] Abrahamsson TR, Jakobsson T, Böttcher MF, Fredrikson M, Jenmalm MC, Björkstén B, Oldaeus G. Probiotics in prevention of IgE-associated eczema: a double-blind, randomized, placebo-controlled trial. The Journal of allergy and clinical immunology 2007;119(5):1174-80
https://pubmed.ncbi.nlm.nih.gov/17349686[5] Agostoni C, Fiocchi A, Riva E, Terracciano L, Sarratud T, Martelli A, Lodi F, D'Auria E, Zuccotti G, Giovannini M. Growth of infants with IgE-mediated cow's milk allergy fed different formulas in the complementary feeding period. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2007;18(7):599-606
https://pubmed.ncbi.nlm.nih.gov/17561927[6] Akobeng AK, Ramanan AV, Buchan I, Heller RF. Effect of breast feeding on risk of coeliac disease: a systematic review and meta-analysis of observational studies. Archives of disease in childhood 2006;91(1):39-43
https://pubmed.ncbi.nlm.nih.gov/16287899[7] Arslanoglu S, Moro GE, Schmitt J, Tandoi L, Rizzardi S, Boehm G. Early dietary intervention with a mixture of prebiotic oligosaccharides reduces the incidence of allergic manifestations and infections during the first two years of life. The Journal of nutrition 2008;138(6):1091-5
https://pubmed.ncbi.nlm.nih.gov/18492839[8] Ascher H, Krantz I, Rydberg L, Nordin P, Kristiansson B. Influence of infant feeding and gluten intake on coeliac disease. Archives of disease in childhood 1997;76(2):113-7
https://pubmed.ncbi.nlm.nih.gov/9068298[9] Auricchio S, Follo D, de Ritis G, Giunta A, Marzorati D, Prampolini L, Ansaldi N, Levi P, Dall'Olio D, Bossi A. Does breast feeding protect against the development of clinical symptoms of celiac disease in children? Journal of pediatric gastroenterology and nutrition 1983;2(3):428-33
https://pubmed.ncbi.nlm.nih.gov/6620050[10] Bardare M, Vaccari A, Allievi E, Brunelli L, Coco F, de Gaspari GC, Flauto U. Influence of dietary manipulation on incidence of atopic disease in infants at risk. Annals of allergy 1993;71(4):366-71
https://pubmed.ncbi.nlm.nih.gov/8214801[11] Barker JM. Clinical review: Type 1 diabetes-associated autoimmunity: natural history, genetic associations, and screening. The Journal of clinical endocrinology and metabolism 2006;91(4):1210-7
https://pubmed.ncbi.nlm.nih.gov/16403820[12] Bateman B, Warner JO, Hutchinson E, Dean T, Rowlandson P, Gant C, Grundy J, Fitzgerald C, Stevenson J. The effects of a double blind, placebo controlled, artificial food colourings and benzoate preservative challenge on hyperactivity in a general population sample of preschool children. Archives of disease in childhood 2004;89(6):506-11
https://pubmed.ncbi.nlm.nih.gov/15155391[13] Bhatia J, Greer F, . Use of soy protein-based formulas in infant feeding. Pediatrics 2008;121(5):1062-8
http://dx.doi.org/10.1542/peds.2008-0564 https://pubmed.ncbi.nlm.nih.gov/18450914[14] Bianchi ML, Bardella MT. Bone and celiac disease. Calcified tissue international 2002;71(6):465-71
https://pubmed.ncbi.nlm.nih.gov/12232681[15] Bock SA. Prospective appraisal of complaints of adverse reactions to foods in children during the first 3 years of life. Pediatrics 1987;79(5):683-8
https://pubmed.ncbi.nlm.nih.gov/3575022[16] Bock SA, Muñoz-Furlong A, Sampson HA. Fatalities due to anaphylactic reactions to foods. The Journal of allergy and clinical immunology 2001;107(1):191-3
https://pubmed.ncbi.nlm.nih.gov/11150011[17] Bourgey M, Calcagno G, Tinto N, Gennarelli D, Margaritte-Jeannin P, Greco L, Limongelli MG, Esposito O, Marano C, Troncone R, Spampanato A, Clerget-Darpoux F, Sacchetti L. HLA related genetic risk for coeliac disease. Gut 2007;56(8):1054-9
https://pubmed.ncbi.nlm.nih.gov/17344279[18] Boyce JA, Assa'a A, Burks AW, Jones SM, Sampson HA, Wood RA, Plaut M, Cooper SF, Fenton MJ, Arshad SH, Bahna SL, Beck LA, Byrd-Bredbenner C, Camargo CA, Eichenfield L, Furuta GT, Hanifin JM, Jones C, Kraft M, Levy BD, Lieberman P, Luccioli S, McCall KM, Schneider LC, Simon RA, Simons FER, Teach SJ, Yawn BP, Schwaninger JM, . Guidelines for the diagnosis and management of food allergy in the United States: summary of the NIAID-Sponsored Expert Panel Report. Nutrition (Burbank, Los Angeles County, Calif.) 2011;27(2):253-67
http://dx.doi.org/10.1016/j.nut.2010.12.001 https://pubmed.ncbi.nlm.nih.gov/21215925[19] , Boyce JA, Assa'ad A, Burks AW, Jones SM, Sampson HA, Wood RA, Plaut M, Cooper SF, Fenton MJ, Arshad SH, Bahna SL, Beck LA, Byrd-Bredbenner C, Camargo CA, Eichenfield L, Furuta GT, Hanifin JM, Jones C, Kraft M, Levy BD, Lieberman P, Luccioli S, McCall KM, Schneider LC, Simon RA, Simons FER, Teach SJ, Yawn BP, Schwaninger JM. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID-sponsored expert panel. The Journal of allergy and clinical immunology 2010;126(6 Suppl):S1-58
http://dx.doi.org/10.1016/j.jaci.2010.10.007 https://pubmed.ncbi.nlm.nih.gov/21134576[20] Suchy FJ, Brannon PM, Carpenter TO, Fernandez JR, Gilsanz V, Gould JB, Hall K, Hui SL, Lupton J, Mennella J, Miller NJ, Osganian SK, Sellmeyer DE, Wolf MA. NIH consensus development conference statement: Lactose intolerance and health. NIH consensus and state-of-the-science statements 2010;27(2):1-27
https://pubmed.ncbi.nlm.nih.gov/20186234[21] Brousse N, Meijer JWR. Malignant complications of coeliac disease. Best practice & research. Clinical gastroenterology 2005;19(3):401-12
https://pubmed.ncbi.nlm.nih.gov/15925845[22] Burks AW, Jones SM, Boyce JA, Sicherer SH, Wood RA, Assa'ad A, Sampson HA. NIAID-sponsored 2010 guidelines for managing food allergy: applications in the pediatric population. Pediatrics 2011;128(5):955-65
http://dx.doi.org/10.1542/peds.2011-0539 https://pubmed.ncbi.nlm.nih.gov/21987705[23] Burks W, Jones SM, Berseth CL, Harris C, Sampson HA, Scalabrin DMF. Hypoallergenicity and effects on growth and tolerance of a new amino acid-based formula with docosahexaenoic acid and arachidonic acid. The Journal of pediatrics 2008;153(2):266-71
http://dx.doi.org/10.1016/j.jpeds.2008.02.043 https://pubmed.ncbi.nlm.nih.gov/18534230[24] Businco L, Dreborg S, Einarsson R, Giampietro PG, Høst A, Keller KM, Strobel S, Wahn U, Björkstén B, Kjellman MN. Hydrolysed cow's milk formulae. Allergenicity and use in treatment and prevention. An ESPACI position paper. European Society of Pediatric Allergy and Clinical Immunology. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1993;4(3):101-11
https://pubmed.ncbi.nlm.nih.gov/8220797[25] Byrne AM, Malka-Rais J, Burks AW, Fleischer DM. How do we know when peanut and tree nut allergy have resolved, and how do we keep it resolved? Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2010;40(9):1303-11
http://dx.doi.org/10.1111/j.1365-2222.2010.03554.x https://pubmed.ncbi.nlm.nih.gov/20645999[26] Caffarelli C, Plebani A, Poiesi C, Petroccione T, Spattini A, Cavagni G. Determination of allergenicity to three cow's milk hydrolysates and an amino acid-derived formula in children with cow's milk allergy. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2002;32(1):74-9
https://pubmed.ncbi.nlm.nih.gov/12002741[27] Carter CM, Urbanowicz M, Hemsley R, Mantilla L, Strobel S, Graham PJ, Taylor E. Effects of a few food diet in attention deficit disorder. Archives of disease in childhood 1993;69(5):564-8
https://pubmed.ncbi.nlm.nih.gov/8257176[28] Cash BD, Schoenfeld P, Chey WD. The utility of diagnostic tests in irritable bowel syndrome patients: a systematic review. The American journal of gastroenterology 2002;97(11):2812-9
https://pubmed.ncbi.nlm.nih.gov/12425553[29] Chafen JJS, Newberry SJ, Riedl MA, Bravata DM, Maglione M, Suttorp MJ, Sundaram V, Paige NM, Towfigh A, Hulley BJ, Shekelle PG. Diagnosing and managing common food allergies: a systematic review. JAMA 2010;303(18):1848-56
http://dx.doi.org/10.1001/jama.2010.582 https://pubmed.ncbi.nlm.nih.gov/20460624[30] Csizmadia CG, Mearin ML, von Blomberg BM, Brand R, Verloove-Vanhorick SP. An iceberg of childhood coeliac disease in the Netherlands. Lancet (London, England) 1999;353(9155):813-4
https://pubmed.ncbi.nlm.nih.gov/10459972[31] de Graaff LCG, Smit JWA, Radder JK. Prevalence and clinical significance of organ-specific autoantibodies in type 1 diabetes mellitus. The Netherlands journal of medicine 2007;65(7):235-47
https://pubmed.ncbi.nlm.nih.gov/17656810[32] de Jong MH, Scharp-Van Der Linden VTM, Aalberse R, Heymans HSA, Brunekreef B. The effect of brief neonatal exposure to cows' milk on atopic symptoms up to age 5. Archives of disease in childhood 2002;86(5):365-9
https://pubmed.ncbi.nlm.nih.gov/11970933[33] de Jong MH, Scharp-van der Linden VT, Aalberse RC, Oosting J, Tijssen JG, de Groot CJ. Randomised controlled trial of brief neonatal exposure to cows' milk on the development of atopy. Archives of disease in childhood 1998;79(2):126-30
https://pubmed.ncbi.nlm.nih.gov/9797592[34] de Vrese M, Schrezenmeir J. Probiotics, prebiotics, and synbiotics. Advances in biochemical engineering/biotechnology 2008;111():1-66
http://dx.doi.org/10.1007/10_2008_097 https://pubmed.ncbi.nlm.nih.gov/18461293[35] Dengate S, Ruben A. Controlled trial of cumulative behavioural effects of a common bread preservative. Journal of paediatrics and child health 2002;38(4):373-6
https://pubmed.ncbi.nlm.nih.gov/12173999[36] Du Toit G, Katz Y, Sasieni P, Mesher D, Maleki SJ, Fisher HR, Fox AT, Turcanu V, Amir T, Zadik-Mnuhin G, Cohen A, Livne I, Lack G. Early consumption of peanuts in infancy is associated with a low prevalence of peanut allergy. The Journal of allergy and clinical immunology 2008;122(5):984-91
http://dx.doi.org/10.1016/j.jaci.2008.08.039 https://pubmed.ncbi.nlm.nih.gov/19000582[37] du Toit G, Meyer R, Shah N, Heine RG, Thomson MA, Lack G, Fox AT. Identifying and managing cow's milk protein allergy. Archives of disease in childhood. Education and practice edition 2010;95(5):134-44
http://dx.doi.org/10.1136/adc.2007.118018 https://pubmed.ncbi.nlm.nih.gov/20688848[38] Egger J, Carter CM, Graham PJ, Gumley D, Soothill JF. Controlled trial of oligoantigenic treatment in the hyperkinetic syndrome. Lancet (London, England) 1985;1(8428):540-5
https://pubmed.ncbi.nlm.nih.gov/2857900[39] Fälth-Magnusson K, Franzén L, Jansson G, Laurin P, Stenhammar L. Infant feeding history shows distinct differences between Swedish celiac and reference children. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1996;7(1):1-5
https://pubmed.ncbi.nlm.nih.gov/8792377[40] Feingold BF. Hyperkinesis and learning disabilities linked to artificial food flavors and colors. The American journal of nursing 1975;75(5):797-803
https://pubmed.ncbi.nlm.nih.gov/1039267[41] Filipiak B, Zutavern A, Koletzko S, von Berg A, Brockow I, Grübl A, Berdel D, Reinhardt D, Bauer CP, Wichmann H-E, Heinrich J, . Solid food introduction in relation to eczema: results from a four-year prospective birth cohort study. The Journal of pediatrics 2007;151(4):352-8
https://pubmed.ncbi.nlm.nih.gov/17889067[42] Fiocchi A, Brozek J, Schünemann H, Bahna SL, von Berg A, Beyer K, Bozzola M, Bradsher J, Compalati E, Ebisawa M, Guzmán MA, Li H, Heine RG, Keith P, Lack G, Landi M, Martelli A, Rancé F, Sampson H, Stein A, Terracciano L, Vieths S, . World Allergy Organization (WAO) Diagnosis and Rationale for Action against Cow's Milk Allergy (DRACMA) Guidelines. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2010;21 Suppl 21():1-125
http://dx.doi.org/10.1111/j.1399-3038.2010.01068.x https://pubmed.ncbi.nlm.nih.gov/20618740[43] Ford AC, Chey WD, Talley NJ, Malhotra A, Spiegel BMR, Moayyedi P. Yield of diagnostic tests for celiac disease in individuals with symptoms suggestive of irritable bowel syndrome: systematic review and meta-analysis. Archives of internal medicine 2009;169(7):651-8
http://dx.doi.org/10.1001/archinternmed.2009.22 https://pubmed.ncbi.nlm.nih.gov/19364994[44] Ford AC, Ching E, Moayyedi P. Meta-analysis: yield of diagnostic tests for coeliac disease in dyspepsia. Alimentary pharmacology & therapeutics 2009;30(1):28-36
http://dx.doi.org/10.1111/j.1365-2036.2009.04008.x https://pubmed.ncbi.nlm.nih.gov/19416130[45] Gijsbers CFM, Kneepkens CMF, Büller HA. Lactose and fructose malabsorption in children with recurrent abdominal pain: results of double-blinded testing. Acta paediatrica (Oslo, Norway : 1992) 2012;101(9):e411-5
http://dx.doi.org/10.1111/j.1651-2227.2012.02721.x https://pubmed.ncbi.nlm.nih.gov/22578243[46] Giuca MR, Cei G, Gigli F, Gandini P. Oral signs in the diagnosis of celiac disease: review of the literature. Minerva stomatologica 2010;59(1-2):33-43
https://pubmed.ncbi.nlm.nih.gov/20212408[47] Goddard CJR, Gillett HR. Complications of coeliac disease: are all patients at risk? Postgraduate medical journal 2006;82(973):705-12
https://pubmed.ncbi.nlm.nih.gov/17099088[48] Gravholt CH. Clinical practice in Turner syndrome. Nature clinical practice. Endocrinology & metabolism 2005;1(1):41-52
https://pubmed.ncbi.nlm.nih.gov/16929365[49] Greco L, Auricchio S, Mayer M, Grimaldi M. Case control study on nutritional risk factors in celiac disease. Journal of pediatric gastroenterology and nutrition 1988;7(3):395-9
https://pubmed.ncbi.nlm.nih.gov/3385552[50] Grossman G. Neurological complications of coeliac disease: what is the evidence? Practical neurology 2008;8(2):77-89
http://dx.doi.org/10.1136/jnnp.2007.139717 https://pubmed.ncbi.nlm.nih.gov/18344378[51] Gutierrez-Achury J, Coutinho de Almeida R, Wijmenga C. Shared genetics in coeliac disease and other immune-mediated diseases. Journal of internal medicine 2011;269(6):591-603
http://dx.doi.org/10.1111/j.1365-2796.2011.02375.x https://pubmed.ncbi.nlm.nih.gov/21401738[52] Haines ML, Anderson RP, Gibson PR. Systematic review: The evidence base for long-term management of coeliac disease. Alimentary pharmacology & therapeutics 2008;28(9):1042-66
http://dx.doi.org/10.1111/j.1365-2036.2008.03820.x https://pubmed.ncbi.nlm.nih.gov/18671779[53] Halmerbauer G, Gartner C, Schier M, Arshad H, Dean T, Koller DY, Karmaus W, Kuehr J, Forster J, Urbanek R, Frischer T, . Study on the prevention of allergy in Children in Europe (SPACE): allergic sensitization in children at 1 year of age in a controlled trial of allergen avoidance from birth. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2002;13(s15):47-54
https://pubmed.ncbi.nlm.nih.gov/12688625[54] Hattevig G, Kjellman B, Sigurs N, Björkstén B, Kjellman NI. Effect of maternal avoidance of eggs, cow's milk and fish during lactation upon allergic manifestations in infants. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 1989;19(1):27-32
https://pubmed.ncbi.nlm.nih.gov/2702510[55] Hays T, Wood RA. A systematic review of the role of hydrolyzed infant formulas in allergy prevention. Archives of pediatrics & adolescent medicine 2005;159(9):810-6
https://pubmed.ncbi.nlm.nih.gov/16143739[56] Heyman MB, . Lactose intolerance in infants, children, and adolescents. Pediatrics 2006;118(3):1279-86
https://pubmed.ncbi.nlm.nih.gov/16951027[57] Hill DJ, Murch SH, Rafferty K, Wallis P, Green CJ. The efficacy of amino acid-based formulas in relieving the symptoms of cow's milk allergy: a systematic review. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2007;37(6):808-22
https://pubmed.ncbi.nlm.nih.gov/17517094[58] Hill ID, Dirks MH, Liptak GS, Colletti RB, Fasano A, Guandalini S, Hoffenberg EJ, Horvath K, Murray JA, Pivor M, Seidman EG, . Guideline for the diagnosis and treatment of celiac disease in children: recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. Journal of pediatric gastroenterology and nutrition 2005;40(1):1-19
https://pubmed.ncbi.nlm.nih.gov/15625418[59] Hogen Esch CE, Rosén A, Auricchio R, Romanos J, Chmielewska A, Putter H, Ivarsson A, Szajewska H, Koning F, Wijmenga C, Troncone R, Mearin ML, . The PreventCD Study design: towards new strategies for the prevention of coeliac disease. European journal of gastroenterology & hepatology 2010;22(12):1424-30
http://dx.doi.org/10.1097/MEG.0b013e32833fe9ae https://pubmed.ncbi.nlm.nih.gov/21389794[60] Husby S, Koletzko S, Korponay-Szabó IR, Mearin ML, Phillips A, Shamir R, Troncone R, Giersiepen K, Branski D, Catassi C, Lelgeman M, Mäki M, Ribes-Koninckx C, Ventura A, Zimmer KP, , , . European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease. Journal of pediatric gastroenterology and nutrition 2012;54(1):136-60
http://dx.doi.org/10.1097/MPG.0b013e31821a23d0 https://pubmed.ncbi.nlm.nih.gov/22197856[61] Huurre A, Laitinen K, Rautava S, Korkeamäki M, Isolauri E. Impact of maternal atopy and probiotic supplementation during pregnancy on infant sensitization: a double-blind placebo-controlled study. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2008;38(8):1342-8
http://dx.doi.org/10.1111/j.1365-2222.2008.03008.x https://pubmed.ncbi.nlm.nih.gov/18477013[62] Iacono G, Carroccio A, Cavataio F, Montalto G, Cantarero MD, Notarbartolo A. Chronic constipation as a symptom of cow milk allergy. The Journal of pediatrics 1995;126(1):34-9
https://pubmed.ncbi.nlm.nih.gov/7815220[63] Ingen-Housz-Oro S. [Dermatitis herpetiformis: a review]. Annales de dermatologie et de venereologie 2011;138(3):221-7
http://dx.doi.org/10.1016/j.annder.2011.01.005 https://pubmed.ncbi.nlm.nih.gov/21397152[64] Isolauri E, Sütas Y, Mäkinen-Kiljunen S, Oja SS, Isosomppi R, Turjanmaa K. Efficacy and safety of hydrolyzed cow milk and amino acid-derived formulas in infants with cow milk allergy. The Journal of pediatrics 1995;127(4):550-7
https://pubmed.ncbi.nlm.nih.gov/7562275[65] Ivarsson A, Hernell O, Stenlund H, Persson LA. Breast-feeding protects against celiac disease. The American journal of clinical nutrition 2002;75(5):914-21
https://pubmed.ncbi.nlm.nih.gov/11976167[66] Jadad AR, Moore RA, Carroll D, Jenkinson C, Reynolds DJ, Gavaghan DJ, McQuay HJ. Assessing the quality of reports of randomized clinical trials: is blinding necessary? Controlled clinical trials 1996;17(1):1-12
https://pubmed.ncbi.nlm.nih.gov/8721797[67] James JM, Bernhisel-Broadbent J, Sampson HA. Respiratory reactions provoked by double-blind food challenges in children. American journal of respiratory and critical care medicine 1994;149(1):59-64
https://pubmed.ncbi.nlm.nih.gov/8111598[68] Järvelä IE. Molecular genetics of adult-type hypolactasia. Annals of medicine 2005;37(3):179-85
https://pubmed.ncbi.nlm.nih.gov/16019716[69] Järvinen KM, Chatchatee P. Mammalian milk allergy: clinical suspicion, cross-reactivities and diagnosis. Current opinion in allergy and clinical immunology 2009;9(3):251-8
http://dx.doi.org/10.1097/ACI.0b013e32832b3f33 https://pubmed.ncbi.nlm.nih.gov/19412090[70] Jellema P, Schellevis FG, van der Windt DAWM, Kneepkens CMF, van der Horst HE. Lactose malabsorption and intolerance: a systematic review on the diagnostic value of gastrointestinal symptoms and self-reported milk intolerance. QJM : monthly journal of the Association of Physicians 2010;103(8):555-72
http://dx.doi.org/10.1093/qjmed/hcq082 https://pubmed.ncbi.nlm.nih.gov/20522486[71] Kajosaari M. Atopy prevention in childhood: the role of diet. Prospective 5-year follow-up of high-risk infants with six months exclusive breastfeeding and solid food elimination. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1994;5(6 Suppl):26-8
https://pubmed.ncbi.nlm.nih.gov/7728225[72] Katz Y, Rajuan N, Goldberg MR, Eisenberg E, Heyman E, Cohen A, Leshno M. Early exposure to cow's milk protein is protective against IgE-mediated cow's milk protein allergy. The Journal of allergy and clinical immunology 2010;126(1):77-82.e1
http://dx.doi.org/10.1016/j.jaci.2010.04.020 https://pubmed.ncbi.nlm.nih.gov/20541249[73] Kerkhof M, Wijga A, Smit HA, de Jongste JC, Aalberse RC, Brunekreef B, Gerritsen J, Postma DS, . The effect of prenatal exposure on total IgE at birth and sensitization at twelve months and four years of age: The PIAMA study. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2005;16(1):10-8
https://pubmed.ncbi.nlm.nih.gov/15693906[74] Klemola T, Vanto T, Juntunen-Backman K, Kalimo K, Korpela R, Varjonen E. Allergy to soy formula and to extensively hydrolyzed whey formula in infants with cow's milk allergy: a prospective, randomized study with a follow-up to the age of 2 years. The Journal of pediatrics 2002;140(2):219-24
https://pubmed.ncbi.nlm.nih.gov/11865274[75] Klemola T, Kalimo K, Poussa T, Juntunen-Backman K, Korpela R, Valovirta E, Vanto T. Feeding a soy formula to children with cow's milk allergy: the development of immunoglobulin E-mediated allergy to soy and peanuts. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2005;16(8):641-6
https://pubmed.ncbi.nlm.nih.gov/16343085[76] Kneepkens CMF, Meijer Y. Clinical practice. Diagnosis and treatment of cow's milk allergy. European journal of pediatrics 2009;168(8):891-6
http://dx.doi.org/10.1007/s00431-009-0955-7 https://pubmed.ncbi.nlm.nih.gov/19271238[77] Kuitunen M, Kukkonen K, Juntunen-Backman K, Korpela R, Poussa T, Tuure T, Haahtela T, Savilahti E. Probiotics prevent IgE-associated allergy until age 5 years in cesarean-delivered children but not in the total cohort. The Journal of allergy and clinical immunology 2009;123(2):335-41
http://dx.doi.org/10.1016/j.jaci.2008.11.019 https://pubmed.ncbi.nlm.nih.gov/19135235[78] Kukkonen K, Savilahti E, Haahtela T, Juntunen-Backman K, Korpela R, Poussa T, Tuure T, Kuitunen M. Probiotics and prebiotic galacto-oligosaccharides in the prevention of allergic diseases: a randomized, double-blind, placebo-controlled trial. The Journal of allergy and clinical immunology 2007;119(1):192-8
https://pubmed.ncbi.nlm.nih.gov/17208601[79] Lack G. Clinical practice. Food allergy. The New England journal of medicine 2008;359(12):1252-60
http://dx.doi.org/10.1056/NEJMcp0800871 https://pubmed.ncbi.nlm.nih.gov/18799559[80] Lannerö E, Wickman M, van Hage M, Bergström A, Pershagen G, Nordvall L. Exposure to environmental tobacco smoke and sensitisation in children. Thorax 2008;63(2):172-6
https://pubmed.ncbi.nlm.nih.gov/18089631[81] Laubereau B, Brockow I, Zirngibl A, Koletzko S, Gruebl A, von Berg A, Filipiak-Pittroff B, Berdel D, Bauer CP, Reinhardt D, Heinrich J, Wichmann H-E, . Effect of breast-feeding on the development of atopic dermatitis during the first 3 years of life--results from the GINI-birth cohort study. The Journal of pediatrics 2004;144(5):602-7
https://pubmed.ncbi.nlm.nih.gov/15126993[82] Lindfors AT, Danielsson L, Enocksson E, Johansson SG, Westin S. Allergic symptoms up to 4-6 years of age in children given cow milk neonatally. A prospective study. Allergy 1992;47(3):207-11
https://pubmed.ncbi.nlm.nih.gov/1510232[83] McCann D, Barrett A, Cooper A, Crumpler D, Dalen L, Grimshaw K, Kitchin E, Lok K, Porteous L, Prince E, Sonuga-Barke E, Warner JO, Stevenson J. Food additives and hyperactive behaviour in 3-year-old and 8/9-year-old children in the community: a randomised, double-blinded, placebo-controlled trial. Lancet (London, England) 2007;370(9598):1560-7
https://pubmed.ncbi.nlm.nih.gov/17825405[84] McCarver G, Bhatia J, Chambers C, Clarke R, Etzel R, Foster W, Hoyer P, Leeder JS, Peters JM, Rissman E, Rybak M, Sherman C, Toppari J, Turner K. NTP-CERHR expert panel report on the developmental toxicity of soy infant formula. Birth defects research. Part B, Developmental and reproductive toxicology 2011;92(5):421-68
http://dx.doi.org/10.1002/bdrb.20314 https://pubmed.ncbi.nlm.nih.gov/21948615[85] Mennella JA, Beauchamp GK. Flavor experiences during formula feeding are related to preferences during childhood. Early human development 2002;68(2):71-82
https://pubmed.ncbi.nlm.nih.gov/12113993[86] Mirzaagha F, Azali SH, Islami F, Zamani F, Khalilipour E, Khatibian M, Malekzadeh R. Coeliac disease in autoimmune liver disease: a cross-sectional study and a systematic review. Digestive and liver disease : official journal of the Italian Society of Gastroenterology and the Italian Association for the Study of the Liver 2010;42(9):620-3
http://dx.doi.org/10.1016/j.dld.2010.02.006 https://pubmed.ncbi.nlm.nih.gov/20236872[87] Moro G, Arslanoglu S, Stahl B, Jelinek J, Wahn U, Boehm G. A mixture of prebiotic oligosaccharides reduces the incidence of atopic dermatitis during the first six months of age. Archives of disease in childhood 2006;91(10):814-9
https://pubmed.ncbi.nlm.nih.gov/16873437[88] Muraro A, Roberts G, Clark A, Eigenmann PA, Halken S, Lack G, Moneret-Vautrin A, Niggemann B, Rancé F, . The management of anaphylaxis in childhood: position paper of the European academy of allergology and clinical immunology. Allergy 2007;62(8):857-71
https://pubmed.ncbi.nlm.nih.gov/17590200[89] Niggemann B, Binder C, Dupont C, Hadji S, Arvola T, Isolauri E. Prospective, controlled, multi-center study on the effect of an amino-acid-based formula in infants with cow's milk allergy/intolerance and atopic dermatitis. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2001;12(2):78-82
https://pubmed.ncbi.nlm.nih.gov/11338290[90] Niggemann B, von Berg A, Bollrath C, Berdel D, Schauer U, Rieger C, Haschke-Becher E, Wahn U. Safety and efficacy of a new extensively hydrolyzed formula for infants with cow's milk protein allergy. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2008;19(4):348-54
http://dx.doi.org/10.1111/j.1399-3038.2007.00653.x https://pubmed.ncbi.nlm.nih.gov/18167160[91] Nova E, Pozo T, Sanz Y, Marcos A. Dietary strategies of immunomodulation in infants at risk for celiac disease. The Proceedings of the Nutrition Society 2010;69(3):347-53
http://dx.doi.org/10.1017/S0029665110001825 https://pubmed.ncbi.nlm.nih.gov/20579407[92] Nowak-Wegrzyn A, Assa'ad AH, Bahna SL, Bock SA, Sicherer SH, Teuber SS, . Work Group report: oral food challenge testing. The Journal of allergy and clinical immunology 2009;123(6 Suppl):S365-83
http://dx.doi.org/10.1016/j.jaci.2009.03.042 https://pubmed.ncbi.nlm.nih.gov/19500710[93] Nowak-Wegrzyn A, Fiocchi A. Rare, medium, or well done? The effect of heating and food matrix on food protein allergenicity. Current opinion in allergy and clinical immunology 2009;9(3):234-7
http://dx.doi.org/10.1097/ACI.0b013e32832b88e7 https://pubmed.ncbi.nlm.nih.gov/19444093[94] Nwaru BI, Erkkola M, Ahonen S, Kaila M, Haapala A-M, Kronberg-Kippilä C, Salmelin R, Veijola R, Ilonen J, Simell O, Knip M, Virtanen SM. Age at the introduction of solid foods during the first year and allergic sensitization at age 5 years. Pediatrics 2010;125(1):50-9
http://dx.doi.org/10.1542/peds.2009-0813 https://pubmed.ncbi.nlm.nih.gov/19969611[95] Odelram H, Vanto T, Jacobsen L, Kjellman NI. Whey hydrolysate compared with cow's milk-based formula for weaning at about 6 months of age in high allergy-risk infants: effects on atopic disease and sensitization. Allergy 1996;51(3):192-5
https://pubmed.ncbi.nlm.nih.gov/8781676[96] Osborn DA, Sinn J. Formulas containing hydrolysed protein for prevention of allergy and food intolerance in infants. The Cochrane database of systematic reviews 2003
https://pubmed.ncbi.nlm.nih.gov/14583987[97] Osborn DA, Sinn J. Soy formula for prevention of allergy and food intolerance in infants. The Cochrane database of systematic reviews 2006;2006(4):CD003741
https://pubmed.ncbi.nlm.nih.gov/17054183[98] Osborn DA, Sinn JK. Prebiotics in infants for prevention of allergic disease and food hypersensitivity. The Cochrane database of systematic reviews 2007
https://pubmed.ncbi.nlm.nih.gov/17943911[99] Pastore L, Carroccio A, Compilato D, Panzarella V, Serpico R, Lo Muzio L. Oral manifestations of celiac disease. Journal of clinical gastroenterology 2008;42(3):224-32
http://dx.doi.org/10.1097/MCG.0b013e318074dd98 https://pubmed.ncbi.nlm.nih.gov/18223505[100] Pelsser LM, Frankena K, Toorman J, Savelkoul HF, Dubois AE, Pereira RR, Haagen TA, Rommelse NN, Buitelaar JK. Effects of a restricted elimination diet on the behaviour of children with attention-deficit hyperactivity disorder (INCA study): a randomised controlled trial. Lancet (London, England) 2011;377(9764):494-503
http://dx.doi.org/10.1016/S0140-6736(10)62227-1 https://pubmed.ncbi.nlm.nih.gov/21296237[101] Pengiran Tengah DSNA, Wills AJ, Holmes GKT. Neurological complications of coeliac disease. Postgraduate medical journal 2002;78(921):393-8
https://pubmed.ncbi.nlm.nih.gov/12151653[102] Perry TT, Matsui EC, Conover-Walker MK, Wood RA. Risk of oral food challenges. The Journal of allergy and clinical immunology 2004;114(5):1164-8
https://pubmed.ncbi.nlm.nih.gov/15536426[103] Peters U, Schneeweiss S, Trautwein EA, Erbersdobler HF. A case-control study of the effect of infant feeding on celiac disease. Annals of nutrition & metabolism 2001;45(4):135-42
https://pubmed.ncbi.nlm.nih.gov/11463995[104] Pumphrey RSH. Fatal anaphylaxis in the UK, 1992-2001. Novartis Foundation symposium 2004;257():116-28; discussion 128-32, 157-60, 276-85
https://pubmed.ncbi.nlm.nih.gov/15025395[105] Pumphrey RSH, Gowland MH. Further fatal allergic reactions to food in the United Kingdom, 1999-2006. The Journal of allergy and clinical immunology 2007;119(4):1018-9
https://pubmed.ncbi.nlm.nih.gov/17349682[106] Rancé F, Kanny G, Dutau G, Moneret-Vautrin DA. Food hypersensitivity in children: clinical aspects and distribution of allergens. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 1999;10(1):33-8
https://pubmed.ncbi.nlm.nih.gov/10410915[107] Rautava S, Kalliomäki M, Isolauri E. Probiotics during pregnancy and breast-feeding might confer immunomodulatory protection against atopic disease in the infant. The Journal of allergy and clinical immunology 2002;109(1):119-21
https://pubmed.ncbi.nlm.nih.gov/11799376[108] Roizen NJ, Patterson D. Down's syndrome. Lancet (London, England) 2003;361(9365):1281-9
https://pubmed.ncbi.nlm.nih.gov/12699967[109] Sainsbury A, Sanders DS, Ford AC. Meta-analysis: Coeliac disease and hypertransaminasaemia. Alimentary pharmacology & therapeutics 2011;34(1):33-40
http://dx.doi.org/10.1111/j.1365-2036.2011.04685.x https://pubmed.ncbi.nlm.nih.gov/21545472[110] Salvatore S, Vandenplas Y. Gastroesophageal reflux and cow milk allergy: is there a link? Pediatrics 2002;110(5):972-84
https://pubmed.ncbi.nlm.nih.gov/12415039[111] Sampson HA, James JM, Bernhisel-Broadbent J. Safety of an amino acid-derived infant formula in children allergic to cow milk. Pediatrics 1992;90(3):463-5
https://pubmed.ncbi.nlm.nih.gov/1518709[112] Sattar N, Lazare F, Kacer M, Aguayo-Figueroa L, Desikan V, Garcia M, Lane A, Chawla A, Wilson T. Celiac disease in children, adolescents, and young adults with autoimmune thyroid disease. The Journal of pediatrics 2011;158(2):272-5.e1
http://dx.doi.org/10.1016/j.jpeds.2010.08.050 https://pubmed.ncbi.nlm.nih.gov/20961564[113] Sausenthaler S, Heinrich J, Koletzko S, . Early diet and the risk of allergy: what can we learn from the prospective birth cohort studies GINIplus and LISAplus? The American journal of clinical nutrition 2011;94(6 Suppl):2012S-2017S
http://dx.doi.org/10.3945/ajcn.110.001180 https://pubmed.ncbi.nlm.nih.gov/21543544[114] Savaiano DA, Boushey CJ, McCabe GP. Lactose intolerance symptoms assessed by meta-analysis: a grain of truth that leads to exaggeration. The Journal of nutrition 2006;136(4):1107-13
https://pubmed.ncbi.nlm.nih.gov/16549489[115] Schab DW, Trinh N-HT. Do artificial food colors promote hyperactivity in children with hyperactive syndromes? A meta-analysis of double-blind placebo-controlled trials. Journal of developmental and behavioral pediatrics : JDBP 2004;25(6):423-34
https://pubmed.ncbi.nlm.nih.gov/15613992[116] Schoetzau A, Filipiak-Pittroff B, Franke K, Koletzko S, Von Berg A, Gruebl A, Bauer CP, Berdel D, Reinhardt D, Wichmann H-E, . Effect of exclusive breast-feeding and early solid food avoidance on the incidence of atopic dermatitis in high-risk infants at 1 year of age. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2002;13(4):234-42
https://pubmed.ncbi.nlm.nih.gov/12390439[117] Schünemann HJ, Oxman AD, Brozek J, Glasziou P, Jaeschke R, Vist GE, Williams JW, Kunz R, Craig J, Montori VM, Bossuyt P, Guyatt GH, . Grading quality of evidence and strength of recommendations for diagnostic tests and strategies. BMJ (Clinical research ed.) 2008;336(7653):1106-10
http://dx.doi.org/10.1136/bmj.39500.677199.AE https://pubmed.ncbi.nlm.nih.gov/18483053[118] Shaukat A, Levitt MD, Taylor BC, MacDonald R, Shamliyan TA, Kane RL, Wilt TJ. Systematic review: effective management strategies for lactose intolerance. Annals of internal medicine 2010;152(12):797-803
http://dx.doi.org/10.7326/0003-4819-152-12-201006150-00241 https://pubmed.ncbi.nlm.nih.gov/20404262[119] Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, Porter AC, Tugwell P, Moher D, Bouter LM. Development of AMSTAR: a measurement tool to assess the methodological quality of systematic reviews. BMC medical research methodology 2007;7():10
https://pubmed.ncbi.nlm.nih.gov/17302989[120] Sigurs N, Hattevig G, Kjellman B. Maternal avoidance of eggs, cow's milk, and fish during lactation: effect on allergic manifestations, skin-prick tests, and specific IgE antibodies in children at age 4 years. Pediatrics 1992;89(4 Pt 2):735-9
https://pubmed.ncbi.nlm.nih.gov/1557270[121] Silano M, Agostoni C, Guandalini S. Effect of the timing of gluten introduction on the development of celiac disease. World journal of gastroenterology 2010;16(16):1939-42
https://pubmed.ncbi.nlm.nih.gov/20419830[122] Snijders BEP, Thijs C, van Ree R, van den Brandt PA. Age at first introduction of cow milk products and other food products in relation to infant atopic manifestations in the first 2 years of life: the KOALA Birth Cohort Study. Pediatrics 2008;122(1):e115-22
http://dx.doi.org/10.1542/peds.2007-1651 https://pubmed.ncbi.nlm.nih.gov/18595956[123] Stallings VA. Calcium and bone health in children: a review. American journal of therapeutics 1997;4(7-8):259-73
https://pubmed.ncbi.nlm.nih.gov/10423619[124] Steens RFR, Csizmadia CGDS, George EK, Ninaber MK, Hira Sing RA, Mearin ML. A national prospective study on childhood celiac disease in the Netherlands 1993-2000: an increasing recognition and a changing clinical picture. The Journal of pediatrics 2005;147(2):239-43
https://pubmed.ncbi.nlm.nih.gov/16126057[125] Syrigou EI, Pitsios C, Panagiotou I, Chouliaras G, Kitsiou S, Kanariou M, Roma-Giannikou E. Food allergy-related paediatric constipation: the usefulness of atopy patch test. European journal of pediatrics 2011;170(9):1173-8
http://dx.doi.org/10.1007/s00431-011-1417-6 https://pubmed.ncbi.nlm.nih.gov/21347849[126] Szajewska H, Mrukowicz JZ, Stoińska B, Prochowska A. Extensively and partially hydrolysed preterm formulas in the prevention of allergic diseases in preterm infants: a randomized, double-blind trial. Acta paediatrica (Oslo, Norway : 1992) 2004;93(9):1159-65
https://pubmed.ncbi.nlm.nih.gov/15384877[127] Szajewska H, Chmielewska A, Pieścik-Lech M, Ivarsson A, Kolacek S, Koletzko S, Mearin ML, Shamir R, Auricchio R, Troncone R, . Systematic review: early infant feeding and the prevention of coeliac disease. Alimentary pharmacology & therapeutics 2012;36(7):607-18
http://dx.doi.org/10.1111/apt.12023 https://pubmed.ncbi.nlm.nih.gov/22905651[128] Szilagyi A, Nathwani U, Vinokuroff C, Correa JA, Shrier I. The effect of lactose maldigestion on the relationship between dairy food intake and colorectal cancer: a systematic review. Nutrition and cancer 2006;55(2):141-50
https://pubmed.ncbi.nlm.nih.gov/17044768[129] Terracciano L, Bouygue GR, Sarratud T, Veglia F, Martelli A, Fiocchi A. Impact of dietary regimen on the duration of cow's milk allergy: a random allocation study. Clinical and experimental allergy : journal of the British Society for Allergy and Clinical Immunology 2010;40(4):637-42
http://dx.doi.org/10.1111/j.1365-2222.2009.03427.x https://pubmed.ncbi.nlm.nih.gov/20067480[130] Tromp IIM, Kiefte-de Jong JC, Lebon A, Renders CM, Jaddoe VWV, Hofman A, de Jongste JC, Moll HA. The introduction of allergenic foods and the development of reported wheezing and eczema in childhood: the Generation R study. Archives of pediatrics & adolescent medicine 2011;165(10):933-8
http://dx.doi.org/10.1001/archpediatrics.2011.93 https://pubmed.ncbi.nlm.nih.gov/21646571[131] van der Aa LB, Heymans HSA, van Aalderen WMC, Sprikkelman AB. Probiotics and prebiotics in atopic dermatitis: review of the theoretical background and clinical evidence. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2010;21(2 Pt 2):e355-67
http://dx.doi.org/10.1111/j.1399-3038.2009.00915.x https://pubmed.ncbi.nlm.nih.gov/19573143[132] van der Windt DAWM, Jellema P, Mulder CJ, Kneepkens CMF, van der Horst HE. Diagnostic testing for celiac disease among patients with abdominal symptoms: a systematic review. JAMA 2010;303(17):1738-46
http://dx.doi.org/10.1001/jama.2010.549 https://pubmed.ncbi.nlm.nih.gov/20442390[133] Vanderhoof JA. Hypoallergenicity and effects on growth and tolerance of a new amino acid-based formula with DHA and ARA. Journal of pediatric gastroenterology and nutrition 2008;47 Suppl 2():S60-1
http://dx.doi.org/10.1097/01.mpg.0000338817.90180.a0 https://pubmed.ncbi.nlm.nih.gov/18931605[134] Venter C, Pereira B, Voigt K, Grundy J, Clayton CB, Higgins B, Arshad SH, Dean T. Prevalence and cumulative incidence of food hypersensitivity in the first 3 years of life. Allergy 2008;63(3):354-9
https://pubmed.ncbi.nlm.nih.gov/18053008[135] von Berg A, Filipiak-Pittroff B, Krämer U, Link E, Bollrath C, Brockow I, Koletzko S, Grübl A, Heinrich J, Wichmann H-E, Bauer C-P, Reinhardt D, Berdel D, . Preventive effect of hydrolyzed infant formulas persists until age 6 years: long-term results from the German Infant Nutritional Intervention Study (GINI). The Journal of allergy and clinical immunology 2008;121(6):1442-7
http://dx.doi.org/10.1016/j.jaci.2008.04.021 https://pubmed.ncbi.nlm.nih.gov/18539195[136] von Berg A, Koletzko S, Filipiak-Pittroff B, Laubereau B, Grübl A, Wichmann H-E, Bauer C-P, Reinhardt D, Berdel D, . Certain hydrolyzed formulas reduce the incidence of atopic dermatitis but not that of asthma: three-year results of the German Infant Nutritional Intervention Study. The Journal of allergy and clinical immunology 2007;119(3):718-25
https://pubmed.ncbi.nlm.nih.gov/17240440[137] West CE, Hammarström M-L, Hernell O. Probiotics during weaning reduce the incidence of eczema. Pediatric allergy and immunology : official publication of the European Society of Pediatric Allergy and Immunology 2009;20(5):430-7
http://dx.doi.org/10.1111/j.1399-3038.2009.00745.x https://pubmed.ncbi.nlm.nih.gov/19298231[138] Willemsen MG, van Valburg RWC, Dirven-Meijer PC, Oranje AP, van der Wouden JC, Moed H. Determining the severity of atopic dermatitis in children presenting in general practice: an easy and fast method. Dermatology research and practice 2009;2009():357046
http://dx.doi.org/10.1155/2009/357046 https://pubmed.ncbi.nlm.nih.gov/20585477[139] Wilt TJ, Shaukat A, Shamliyan T, Taylor BC, MacDonald R, Tacklind J, Rutks I, Schwarzenberg SJ, Kane RL, Levitt M. Lactose intolerance and health. Evidence report/technology assessment 2010
https://pubmed.ncbi.nlm.nih.gov/20629478[140] Wolraich ML, Wilson DB, White JW. The effect of sugar on behavior or cognition in children. A meta-analysis. JAMA 1995;274(20):1617-21
https://pubmed.ncbi.nlm.nih.gov/7474248[141] Wood RA. The natural history of food allergy. Pediatrics 2003;111(6 Pt 3):1631-7
https://pubmed.ncbi.nlm.nih.gov/12777603[142] Zutavern A, Brockow I, Schaaf B, Bolte G, von Berg A, Diez U, Borte M, Herbarth O, Wichmann H-E, Heinrich J, . Timing of solid food introduction in relation to atopic dermatitis and atopic sensitization: results from a prospective birth cohort study. Pediatrics 2006;117(2):401-11
https://pubmed.ncbi.nlm.nih.gov/16452359[143] Zutavern A, Brockow I, Schaaf B, von Berg A, Diez U, Borte M, Kraemer U, Herbarth O, Behrendt H, Wichmann H-E, Heinrich J, . Timing of solid food introduction in relation to eczema, asthma, allergic rhinitis, and food and inhalant sensitization at the age of 6 years: results from the prospective birth cohort study LISA. Pediatrics 2008;121(1):e44-52
http://dx.doi.org/10.1542/peds.2006-3553 https://pubmed.ncbi.nlm.nih.gov/18166543[144] Zutavern A, von Mutius E, Harris J, Mills P, Moffatt S, White C, Cullinan P. The introduction of solids in relation to asthma and eczema. Archives of disease in childhood 2004;89(4):303-8
https://pubmed.ncbi.nlm.nih.gov/15033835[145] Anonymous (2007). Artificial colors and hyperactivity
http://www.food.gov.uk.[146] Anonymous (2008a). Diagnostiek van Koemelkallergie in Nederland: Anders.
[147] Anonymous (2008b). Verordening EG 1333/2008. In (Anonymous).
http://Eur-lex.europa.eu.[148] Anonymous (2011). Multidisciplinaire richtlijn: Excessief huilen bij zuigelingen (in ontwikkeling). In (Anonymous). TNO, Leiden.
[149] CBO (2006). Richtlijn Constitutioneel eczeem.
[150] CBO (2008). Richtlijn Coeliakie en Dermatitis Herpetiformis.
[151] Chafen JJS, Newberry SJ, Riedl M, Bravata DM, Maglione MA, Booth M, Sundaram V, Paige NM, Towfigh A, Hulley BJ, Shekelle PG. Prevalence, Natural History, Diagnosis, and Treatment of Food Allergy: A Systematic Review of the Evidence (null) 2010
https://www.rand.org/pubs/working_papers/WR757-1.html[152] Büchner FL, Ezendam J, Tijhuis MJ, Mennes W, van Loveren H, van den Berg SW. Voeding en ADHD Diet and ADHD 2010
[153] Commissie ‘Standaard’. Landelijke standaard voor de diagnose en behandeling van voedselovergevoeligheid bij zuigelingen op het consultatiebureau. LIVO: Den Haag. 1994
[154] Gezondheidsraad. Voedselallergie 2007
[155] Kamphuis M.. JGZ-richtlijn Huidafwijkingen. 2012
http://www.ncj.nl/bibliotheek/%20richtlijnen/[156] Kneepkens CMF, van Drongelen KI, Aarsen CJE. Landelijke standaard voedselallergie bij zuigelingen; standaard voor de diagnose, behandeling en preventie van voedselallergie bij zuigelingen op het consultatiebureau. In (Anonymous). 2005
[157] Kramer MS, Kakuma R. Maternal dietary antigen avoidance during pregnancy or lactation, or both, for preventing or treating atopic disease in the child. The Cochrane database of systematic reviews 2012;2012(9):CD000133
http://dx.doi.org/10.1002/14651858.CD000133.pub3 https://pubmed.ncbi.nlm.nih.gov/22972039[158] Lucassen P. Colic in infants. BMJ clinical evidence 2010;2010():
https://pubmed.ncbi.nlm.nih.gov/21729336[159] Lucassen P, Albeda F, van Reisen M, Silvius A, Wensing C, Luning-Koster M. M47NHG-Standaard Voedselovergevoeligheid Huisarts En Wetenschap 2010;53():537
http://dx.doi.org/10.1007/BF03089284[160] Meijer Y., Brand P.L.P., Duijvestijn Y.C.M., Vlieg-Boerstra B.J.. Diagnostiek naar voedselallergie in de tweede lijn: Consensusstandpunt sectie kinderallergologie. Tijdschrift voor Kindergeneeskunde, 78(6), 237-243. 2010
https://doi.org/10.1007/s12456-010-0057-5[161] Mofidi S., Bock S.A.. The Food Allergy & Anaphylaxis Network. A Health professional’s guide to food challenges. In (Anonymous). 2005
[162] National Institute for Health and Clinical Excellence (NICE). Coeliac disease. Recognition and assessment of coeliac disease. Clinical Guideline. 2009
[163] National Institute for Health and Clinical Excellence. (2011). NICE clinical guideline 116 – Food allergy in children and young people National Institute for Health and Clinical Excellence (2011). Diagnosis and assessment of food allergy in children and young people in primary care and community settings. In (Anonymous), London. 2011
[164] Olives J-P. [When should we introduce gluten into the feeding of the new-born babies?]. Archives de pediatrie : organe officiel de la Societe francaise de pediatrie 2010;17 Suppl 5():S199-203
http://dx.doi.org/10.1016/S0929-693X(10)70927-1 https://pubmed.ncbi.nlm.nih.gov/21300263[165] RIVM. Rijksvaccinatieprogramma. 2012
[166] Sprikkelman A., Vlieg-Boerstra B., Kneepkens C.. Diagnostiek van Koemelkallergie bij kinderen in Nederland. Utrecht, Nederlandse Vereniging voor Kindergeneeskunde. 2012
http://www.nvk.nl[167] Stichting Nationaal Programma Grieppreventie (2012). In (Anonymous).
[168] van den Berg S.W., Büchner F.L., Boer J.M.A., Ezendam J., Mennes W., van Loveren H., Verhagen H.. Voeding en ADHD: beoordeling van de INCA-studie. Bilthoven. 2011
[169] Vlieg-Boerstra BJ, Meijer Y.. Dubbelblinde voedselprovocaties Tijdschrift voor Kindergeneeskunde 2008;76(2):66
http://dx.doi.org/10.1007/BF03078182 https://doi.org/10.1007/BF03078182Heb je suggesties voor verbetering van deze JGZ-richtlijn?
Geef jouw feedbackLET OP: print de JGZ-richtlijn in liggende afdrukstand!
Grote tabellen zijn niet volledig zichtbaar als de JGZ-richtlijn in staande afdrukstand geprint wordt. Om kleuren in de printversie goed door te laten komen, moet bij de printerinstellingen Achtergrondillustraties aangezet worden.
Disclaimer printversie JGZ-richtlijnen
De printversie van de JGZ-richtlijn bevat de algemene tekst inclusief de aanbevelingen. De wetenschappelijke onderbouwing is terug te vinden op de website, bij de aanbevelingen onder de link “Evidence”.